inlärningsmål
- State hunds regel.
- applicera hunds regel på fyllning av orbitaler.
- använd orbitalfyllningsdiagram för att beskriva placeringen av elektroner i en atom.
har du någonsin undrat vad dessa lastgräns tecken betyder på en bro?
tecknet ovan säger att ingenting över fem ton är tillåtet eftersom det kommer att skada strukturen., Det finns gränser för den vikt som en bro kan stödja, det finns gränser för antalet personer som säkert kan uppta ett rum, och det finns gränser för vad som kan gå in i en elektron orbital.

hunds regel
den sista av de tre reglerna för att konstruera elektronarrangemang kräver att elektroner placeras en i taget i en uppsättning orbitaler inom samma undernivå. Detta minimerar de naturliga repulsiva krafter som en elektron har för en annan., Hunds regel säger att orbitaler med lika energi är alla upptagna av en elektron innan någon orbital upptas av en andra elektron och att var och en av de enskilda elektronerna måste ha samma spinn. Figuren nedan visar hur en uppsättning av tre p orbitaler är fylld med en, två, tre och fyra elektroner.
Orbitalfyllningsdiagram
ett orbitalfyllningsdiagram är det mer visuella sättet att representera arrangemanget av alla elektroner i en viss atom., I ett orbitalfyllningsdiagram visas de enskilda orbitalerna som cirklar (eller kvadrater) och orbitaler inom en undernivå dras bredvid varandra horisontellt. Varje undernivå är märkt med dess huvudsakliga energinivå och undernivå. Elektroner indikeras med pilar inuti cirklarna. En pil som pekar uppåt indikerar en spinriktning, medan en nedåtgående pekande pil indikerar den andra riktningen. De orbitala fyllningsdiagrammen för väte, helium och litium visas i figur nedan.
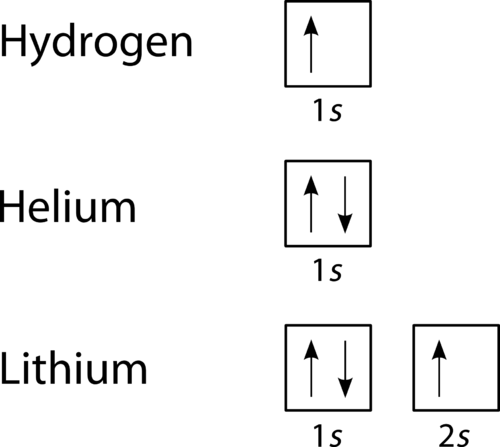
Figur 2., Orbital fyllningsdiagram för väte, helium och litium.
enligt Aufbau-processen fylls undernivåer och orbitaler med elektroner för att öka energin. Eftersom s-undernivån består av bara en orbital, parar den andra elektronen helt enkelt upp med den första elektronen som i helium. Nästa element är litium och kräver användning av nästa tillgängliga undernivå, 2s.
fyllningsdiagrammet för kol visas i figuren nedan. Det finns två 2 p elektroner för kol och var och en upptar sin egen 2 p orbital.,
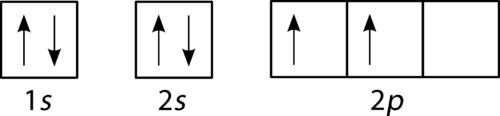
Figur 3. Orbital fyllningsdiagram för kol.
syre har fyra 2 p elektroner. Efter varje 2 p orbital har en elektron i det, den fjärde elektronen kan placeras i den första 2 p orbital med en spin motsatt den andra elektronen i den orbital.
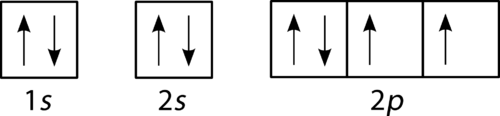
Figur 4. Orbital fyllningsdiagram för syre.
sammanfattning
- hunds regel anger ordningen för elektronfyllning inom en uppsättning orbitaler.,
- Orbital fyllningsdiagram är ett sätt att indikera elektronplatser i orbitaler.
öva
använd länken nedan för att utföra följande övning:
https://www.caymanchem.com/app/template/chemAssistant,verktyg.vm / itemid/4001
- välj en atom från listan (du kommer förmodligen att vilja göra lägre atomnummer). Lämna numret noll.
- slå upp atomen på ett periodiskt bord och bestämma antalet elektroner närvarande.
- Rita orbitalfyllningsdiagrammet för atomen.,
- Klicka på ”Beräkna” – knappen och jämföra ditt svar med den som tillhandahålls.
granska
- State hunds regel.
- Vad är ett orbitalfyllningsdiagram?
- är diagrammet i figuren nedan korrekt? Förklara ditt svar.

- är diagrammet i figuren nedan korrekt? Förklara ditt svar.,

ordlista
- hunds regel: orbitaler med lika energi upptas av en elektron innan någon orbital upptas av en andra elektron och att var och en av de enskilda elektronerna måste ha samma spinn.
- orbital fyllningsdiagram: ett visuellt sätt att representera arrangemanget av alla elektroner i en viss atom.