lärandemål
i slutet av detta avsnitt kommer du att kunna:
- förklara hur energi kan härledas från fett
- förklara syftet och processen med ketogenes
- beskriv processen med ketonkroppsoxidation
- förklara syftet och processen med lipogenes
fetter (eller triglycerider) i kroppen intas som mat eller syntetiseras av adipocyter eller hepatocyter från Kolhydratprekursorer., Lipidmetabolism medför oxidation av fettsyror för att antingen generera energi eller syntetisera nya lipider från mindre ingående molekyler. Lipidmetabolism är associerad med kolhydratmetabolism, eftersom produkter av glukos (såsom acetyl CoA) kan omvandlas till lipider.

Figur 1. En triglyceridmolekyl (a) bryts ned till en monoglycerid (b).,
lipidmetabolism börjar i tarmen där intagna triglycerider bryts ner i mindre kedjiga fettsyror och därefter in i monoglyceridmolekyler genom pankreatiska lipaser, enzymer som bryter ner fetter efter att de emulgeras av gallsalter. När mat når tunntarmen i form av chym, frigörs ett matsmältningshormon som kallas cholecystokinin (CCK) av tarmceller i tarmslimhinnan., CCK stimulerar frisättningen av pankreaslipas från bukspottkörteln och stimulerar sammandragningen av gallblåsan för att frigöra lagrade gallsalter i tarmarna. CCK reser också till hjärnan, där den kan fungera som en hunger suppressant.

Figur 2. Chylomikroner innehåller triglycerider, kolesterolmolekyler och andra apolipoproteiner (proteinmolekyler)., De fungerar för att bära dessa vattenolösliga molekyler från tarmen, genom lymfsystemet och in i blodomloppet, som bär lipiderna till fettvävnad för lagring.
tillsammans bryter pankreaslipaserna och gallsalterna ner triglycerider till fria fettsyror. Dessa fettsyror kan transporteras över tarmmembranet. Men när de passerar membranet rekombineras de för att återigen bilda triglyceridmolekyler., Inom tarmcellerna förpackas dessa triglycerider tillsammans med kolesterolmolekyler i fosfolipidblåsor som kallas chylomikroner. Chylomikronerna gör det möjligt för fetter och kolesterol att röra sig inom vattenmiljön i dina lymfatiska och cirkulationssystem. Chylomikroner lämnar enterocyterna genom exocytos och går in i lymfsystemet via laktealer i tarmens villi. Från lymfsystemet transporteras chylomikronerna till cirkulationssystemet., En gång i cirkulationen kan de antingen gå till levern eller lagras i fettceller (adipocyter) som innefattar fett (fett) vävnad som finns i hela kroppen.
lipolys
för att få energi från fett måste triglycerider först delas upp genom hydrolys i deras två huvudkomponenter, fettsyror och glycerol. Denna process, kallad lipolys, sker i cytoplasman. De resulterande fettsyrorna oxideras genom β-oxidation till acetyl CoA, som används av Krebs-cykeln., Glycerolen som frigörs från triglycerider efter lipolys går direkt in i glykolysvägen som DHAP. Eftersom en triglyceridmolekyl ger tre fettsyramolekyler med så mycket som 16 eller fler kol i var och en, ger fettmolekyler mer energi än kolhydrater och är en viktig energikälla för människokroppen. Triglycerider ger mer än dubbelt så mycket energi per massenhet jämfört med kolhydrater och proteiner. Därför, när glukosnivåerna är låga, triglycerider kan omvandlas till acetyl CoA molekyler och används för att generera ATP genom aerob andning.,
nedbrytningen av fettsyror, som kallas fettsyraoxidation eller beta (β)-oxidation, börjar i cytoplasman, där fettsyror omvandlas till fettsyracoa-molekyler. Denna feta acyl CoA kombinerar med karnitin för att skapa en fet acylkarnitinmolekyl, vilket hjälper till att transportera fettsyran över mitokondrialmembranet. Väl inne i den mitokondriella matrisen omvandlas fett-acylkarnitinmolekylen tillbaka till fet acyl CoA och sedan till acetyl CoA., Den nybildade acetyl CoA går in i Krebs-cykeln och används för att producera ATP på samma sätt som acetyl CoA härrörande från pyruvat.

Figur 3. Klicka för en större bild. Under fettsyraoxidation kan triglycerider brytas ner i acetyl CoA-molekyler och användas för energi när glukosnivåerna är låga.
ketogenes
om överdriven acetyl CoA skapas från oxidationen av fettsyror och Krebs-cykeln är överbelastad och inte kan hantera den, leds acetyl CoA för att skapa ketonkroppar., Dessa ketonkroppar kan fungera som bränslekälla om glukosnivåerna är för låga i kroppen. Ketoner tjänar som bränsle i tider av långvarig svält eller när patienter lider av okontrollerad diabetes och inte kan utnyttja det mesta av den cirkulerande glukosen. I båda fallen befrias fettbutiker för att generera energi genom Krebs-cykeln och kommer att generera ketonkroppar när för mycket acetyl CoA ackumuleras.
i denna ketonsyntesreaktion omvandlas överskott av acetyl CoA till hydroximetylglutaryl CoA (HMG CoA)., HMG CoA är en föregångare till kolesterol och är en mellanprodukt som därefter omvandlas till β-hydroxibutyrat, den primära ketonkroppen i blodet.

Figur 4. Överskott av acetyl CoA avleds från Krebs-cykeln till ketogenesvägen. Denna reaktion uppträder i levercellernas mitokondrier. Resultatet är produktionen av β-hydroxibutyrat, den primära ketonkroppen som finns i blodet.,
Ketonkroppsoxidation
organ som klassiskt tros vara beroende enbart av glukos, såsom hjärnan, kan faktiskt använda ketoner som en alternativ energikälla. Detta håller hjärnan fungerar när glukos är begränsad. När ketoner produceras snabbare än de kan användas kan de brytas ner i CO2 och aceton. Aceton avlägsnas genom utandning. Ett symptom på ketogenes är att patientens andetag luktar sött som alkohol. Denna effekt ger ett sätt att berätta om en diabetiker kontrollerar sjukdomen ordentligt., Den producerade koldioxiden kan surgöra blodet, vilket leder till diabetisk ketoacidos, ett farligt tillstånd hos diabetiker.
ketoner oxiderar för att producera energi för hjärnan. beta (β)-hydroxibutyrat oxideras till acetoacetat och NADH frigörs. En HS-CoA-molekyl tillsätts acetoacetat och bildar acetoacetyl CoA. Kolet i acetoacetyl CoA som inte är bunden till CoA sedan lossnar, dela upp molekylen i två. Detta kol fäster sedan till en annan fri HS-CoA, vilket resulterar i två acetyl CoA molekyler., Dessa två acetyl CoA-molekyler bearbetas sedan genom Krebs-cykeln för att generera energi.

Figur 5. När glukos är begränsad kan ketonkroppar oxideras för att producera acetyl CoA som ska användas i Krebs-cykeln för att generera energi.
lipogenes
när glukosnivåerna är rikliga kan överskott av acetyl CoA som genereras av glykolys omvandlas till fettsyror, triglycerider, kolesterol, steroider och gallsalter., Denna process, som kallas lipogenes, skapar lipider (fett) från acetyl CoA och sker i cytoplasman hos adipocyter (fettceller) och hepatocyter (leverceller). När du äter mer glukos eller kolhydrater än din kropp behöver, använder ditt system acetyl CoA för att göra överskottet till fett. Även om det finns flera metaboliska källor till acetyl CoA, är det oftast härledd från glykolys. Acetyl CoA tillgänglighet är signifikant, eftersom den initierar lipogenes., Lipogenes börjar med acetyl CoA och avancerar genom efterföljande tillsats av två kolatomer från en annan acetyl CoA; denna process upprepas tills fettsyror är lämplig längd. Eftersom detta är en bindningsskapande anabolisk process förbrukas ATP. Skapandet av triglycerider och lipider är dock ett effektivt sätt att lagra den energi som finns tillgänglig i kolhydrater. Triglycerider och lipider, högenergimolekyler, lagras i fettvävnad tills de behövs.,
även om lipogenes uppträder i cytoplasman, skapas den nödvändiga acetyl-CoA i mitokondrierna och kan inte transporteras över mitokondriembranet. För att lösa detta problem omvandlas pyruvat till både oxaloacetat och acetyl CoA. Två olika enzymer krävs för dessa omvandlingar. Oxaloacetat bildas via verkan av pyruvatkarboxylas, medan verkan av pyruvatdehydrogenas skapar acetyl CoA. Oxaloacetat och acetyl CoA kombineras för att bilda citrat, vilket kan korsa mitokondrialmembranet och komma in i cytoplasman., I cytoplasman omvandlas citrat tillbaka till oxaloacetat och acetyl CoA. Oxaloacetat omvandlas till malat och sedan till pyruvat. Pyruvat korsar tillbaka över det mitokondriella membranet för att vänta på nästa cykel av lipogenes. Acetyl CoA omvandlas till malonyl CoA som används för att syntetisera fettsyror. Figur 6 sammanfattar vägarna för lipidmetabolism.
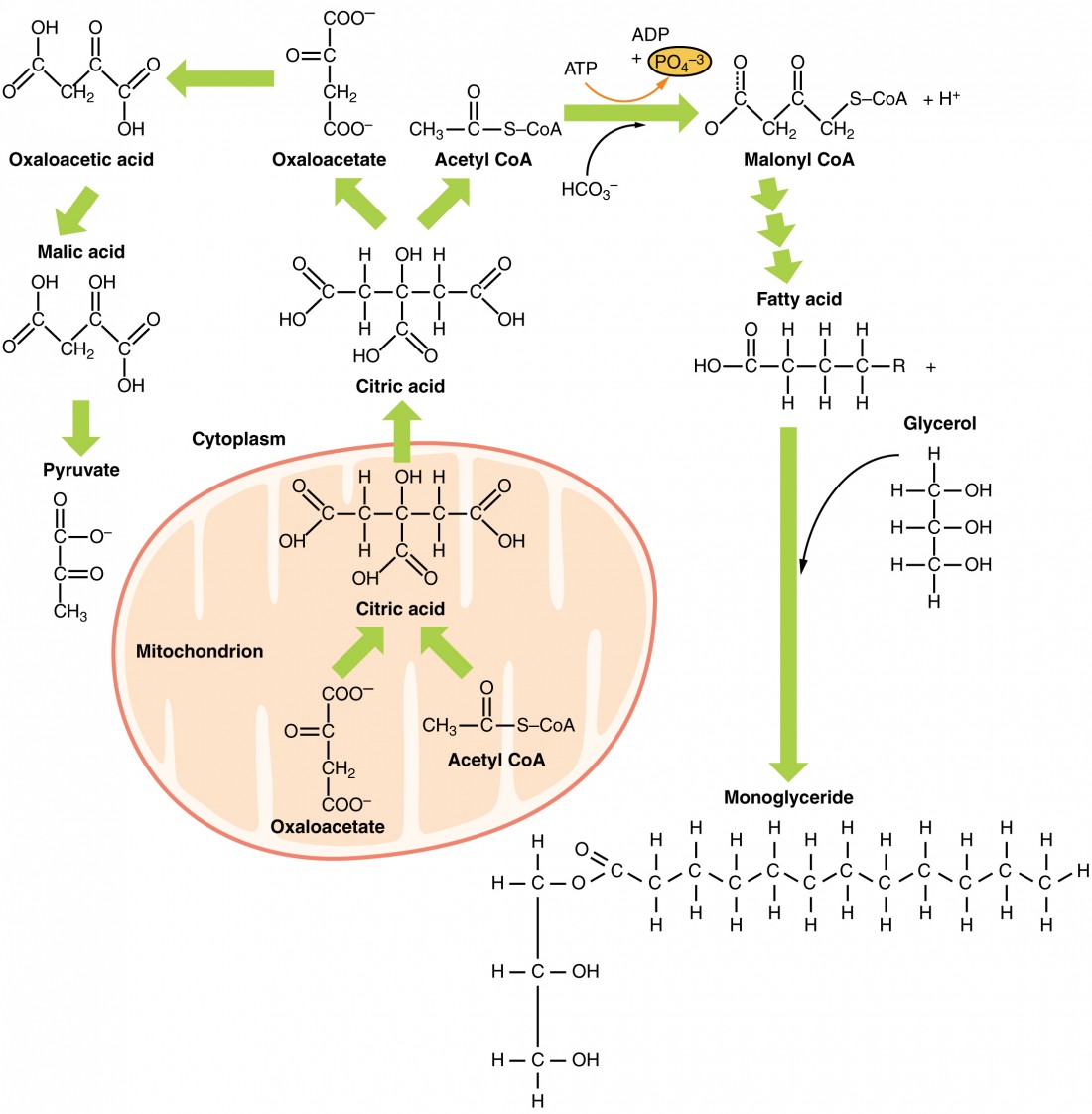
Figur 6. Lipider kan följa en av flera vägar under ämnesomsättningen. Glycerol och fettsyror följer olika vägar.,
Kapitel översyn
lipider är tillgängliga för kroppen från tre källor. De kan intas i kosten, lagras i kroppens fettvävnad eller syntetiseras i levern. Fetter som tas in i kosten smälts i tunntarmen. Triglyceriderna bryts ner i monoglycerider och fria fettsyror och importeras sedan över tarmslimhinnan. En gång över, triglycerider återsyntes och transporteras till levern eller fettvävnad., Fettsyror oxideras genom fettsyra eller β-oxidation i två-kolacetyl CoA-molekyler, som sedan kan komma in i Krebs-cykeln för att generera ATP. Om överskott av acetyl CoA skapas och överbelastar kapaciteten hos Krebs-cykeln, kan acetyl CoA användas för att syntetisera ketonkroppar. När glukos är begränsad kan ketonkroppar oxideras och användas för bränsle. Överskott av acetyl CoA som genereras från överskott av glukos eller kolhydratintag kan användas för fettsyrasyntes eller lipogenes. Acetyl CoA används för att skapa lipider, triglycerider, steroidhormoner, kolesterol och gallsalter., Lipolys är nedbrytningen av triglycerider i glycerol och fettsyror, vilket gör dem lättare för kroppen att bearbeta.
självkontroll
svara på frågorna nedan för att se hur bra du förstår de ämnen som omfattas av föregående avsnitt.
kritiska tänkande frågor
- diskutera hur kolhydrater kan lagras som fett.
- om en diabetes andedräkt luktar alkohol, Vad kan det betyda?