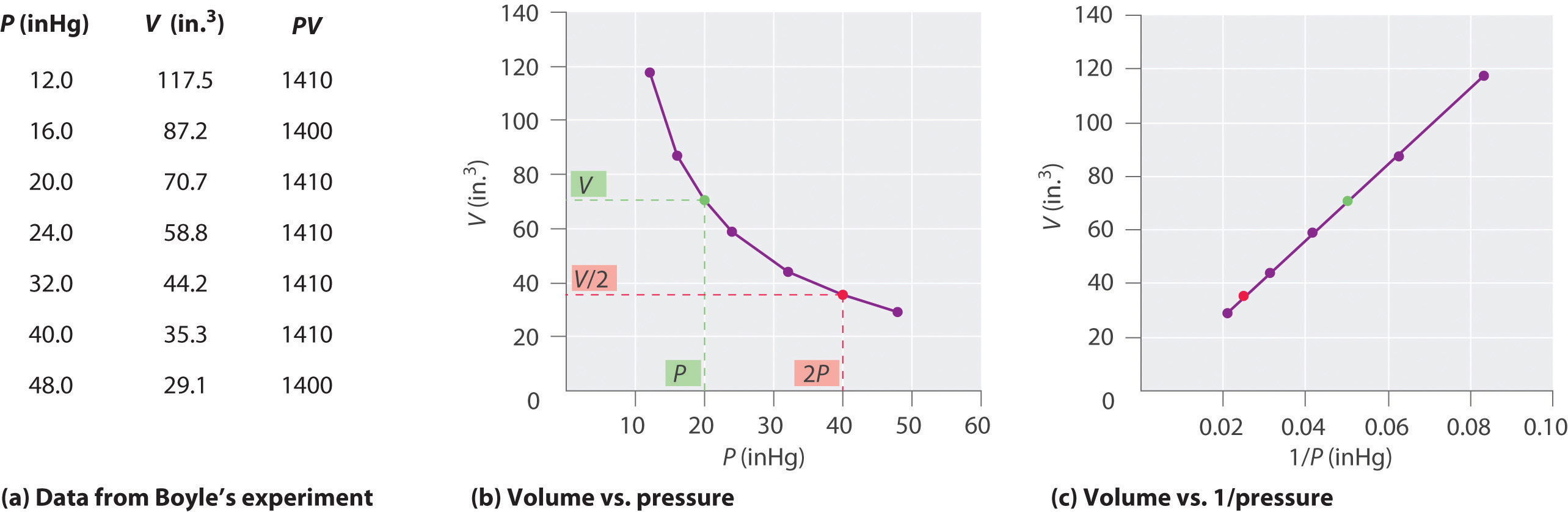
förhållandet mellan tryck och volym: Boyles lag
När trycket på en gas ökar minskar gasvolymen eftersom gaspartiklarna tvingas närmare varandra. Omvänt, när trycket på en gas minskar, ökar gasvolymen eftersom gaspartiklarna nu kan röra sig längre ifrån varandra., Väderballonger blir större när de stiger genom atmosfären till regioner med lägre tryck eftersom gasvolymen har ökat. det vill säga den atmosfäriska gasen utövar mindre tryck på ballongens yta, så den inre gasen expanderar tills det inre och yttre trycket är lika.
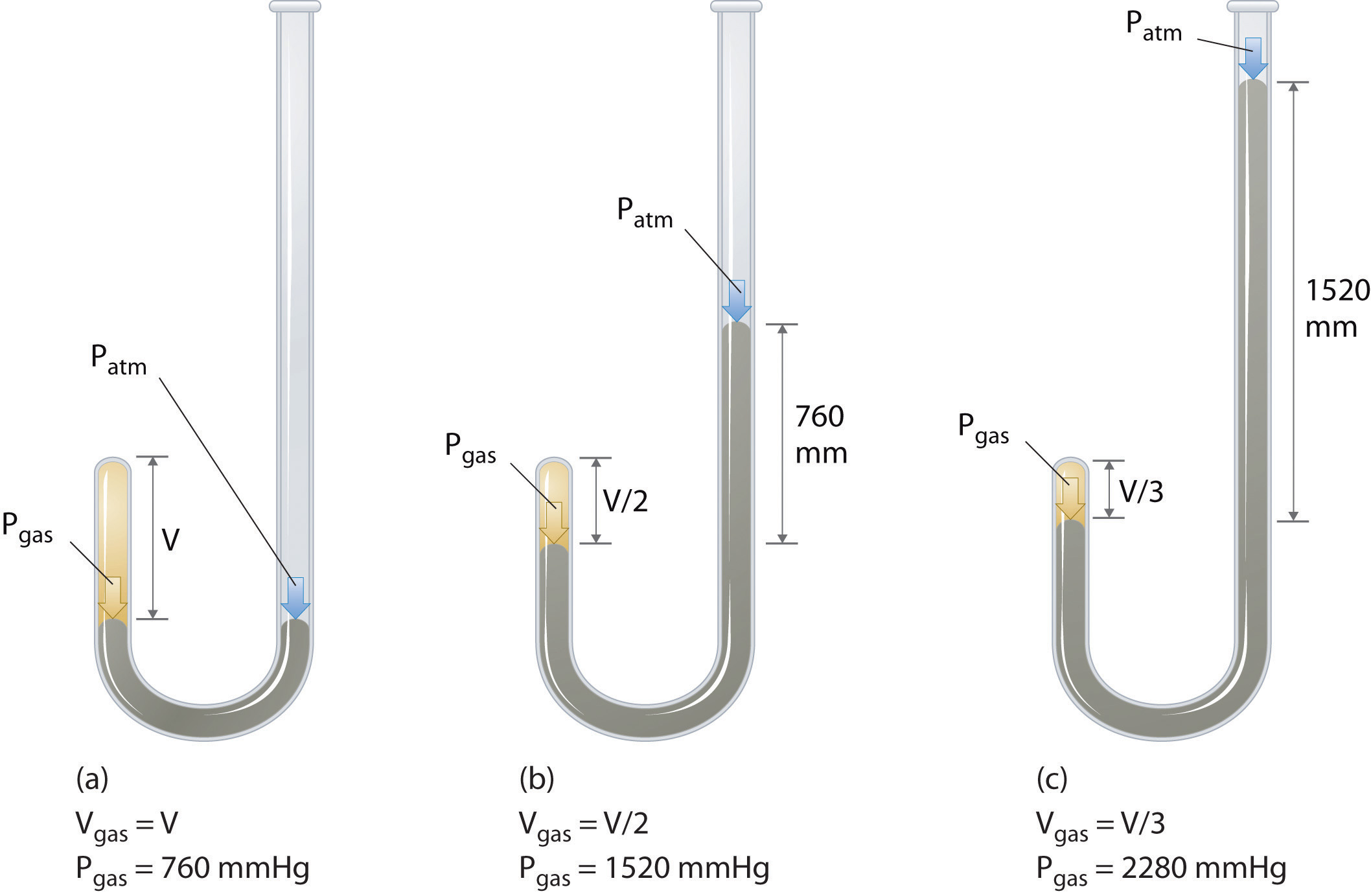
den irländska kemisten Robert Boyle (1627-1691) utförde några av de tidigaste experimenten som bestämde det kvantitativa förhållandet mellan trycket och volymen av en gas. Boyle använde ett J-format rör delvis fyllt med kvicksilver, som visas i Figur \(\PageIndex{1}\)., I dessa experiment fångas en liten mängd gas eller luft över kvicksilverkolonnen, och dess volym mäts vid atmosfärstryck och konstant temperatur. Mer kvicksilver hälls sedan i den öppna armen för att öka trycket på gasprovet. Trycket på gasen är atmosfärstryck plus skillnaden i kvicksilverkolonnernas höjder och den resulterande volymen mäts. Denna process upprepas tills det inte finns något mer utrymme i den öppna armen eller gasvolymen är för liten för att mätas noggrant., Data som de från ett av Boyles egna experiment kan ritas på flera sätt (figur \(\PageIndex{2}\)). En enkel plot av \(v\) versus \ (P\) ger en kurva som kallas en hyperbola och avslöjar ett omvänt förhållande mellan tryck och volym: när trycket fördubblas minskar volymen med en faktor av två. Detta förhållande mellan de två mängderna beskrivs enligt följande:
\
att dela båda sidorna med \(p\) ger en ekvation som illustrerar det inversa förhållandet mellan \(p\) och \(v\):
\
eller
\
där symbolen läses ”är proportionell mot.”Ett diagram av V mot 1 / P är således en rak linje vars lutning är lika med konstanten i ekvation 6.2.1 och ekvation 6.2.3. Att dela båda sidorna av ekvation 6.2.1 med V istället för P ger ett liknande förhållande mellan P och 1 / V., Det numeriska värdet av konstanten beror på mängden gas som används i experimentet och på den temperatur vid vilken experimenten utförs. Detta förhållande mellan tryck och volym är känt som Boyles lag, efter upptäckaren, och kan anges enligt följande: vid konstant temperatur är volymen av en fast mängd gas omvänt proportionell mot dess tryck.