introduktion
typ 2 diabetes mellitus (T2DM) kännetecknas av en insulinresistens, som förblir relativt stabil under hela sjukdomsförloppet, och en progressiv förlust av β-cellfunktion med otillräcklig insulinsekretion., På grund av denna progressiva utveckling kommer de flesta patienter med T2DM så småningom att kräva insulin för att uppnå och upprätthålla glykemisk kontroll, med hjälp av ett stegvis tillvägagångssätt som börjar med basinsulin kombinerat med orala medel. När Pre-prandial och postprandial glykemi inte kontrolleras tillräckligt, föredras en två gånger dagligen insulinbehandling med NPH (Neutral protamin Hagedorn) eller förblandade insulinpreparat som nästa steg., Liksom hos typ 1-diabetiker bör basal-bolusinsulinbehandling vara indicerad hos T2DM-patienter med svår insulinbrist som inte kan uppnå och upprätthålla glykemiska mål med två gånger dagligen.1 Denna insulinregim är dock klart underutnyttjad förmodligen på grund av motviljan hos patienter och läkare på grund av komplexiteten i dess etablering samt den begränsade information som finns tillgänglig om genomförbarheten, särskilt hos äldre personer, och dess effekt hos patienter som tidigare behandlats med två insulindoser.,2
i denna studie utvärderade vi genomförbarheten, effektiviteten och säkerheten av basal-bolusinsulinterapi hos patienter med långvarig typ 2-diabetes och dålig eller instabil glykemisk kontroll.
Material och metoder
i denna prospektiva singelcenterstudie tog vi in 37 patienter som byttes till basal-bolusinsulinbehandling från oktober 2006 till oktober 2007 och hade haft instabil eller dålig glykemisk kontroll (glykerat hemoglobin (HbA1c)≥8%) under de senaste sex månaderna, trots insatser för att förbättra den., Studieprotokollet godkändes av institutions ethics review boards och informerat skriftligt samtycke erhölls från alla patienter.
i den ursprungliga behandlingen distribuerades kolhydrater i de tre huvudmåltiderna. Den initiala insulin glargindosen beräknades som 50% av den tidigare totala dagliga dosen och det initiala prandiala insulinet (aspart eller lispro) som resterande 50% av den totala dagliga dosen, som delades lika för att täcka de tre måltiderna., Patienter som tog metformin innan de bytte behandling och inte hade någon kontraindikation för det, fortsatte att använda det i samma dos. De andra orala antidiabetika stoppades.
alla patienter deltog i ett strukturerat outpatientdiabetes träningsprogram bestående av tre 2-h-gruppsessioner på en vecka för 5-8 patienter. I allmänhet lärdes de att följa en diet som antar kvalitativt kolhydratintag vid varje måltid, men för patienter som ville variera det måste kolhydraträkning göras., Patienterna lärde sig också hanteringen av basal-bolusbehandlingen och hur man justerar basalinsulindoserna enligt fastande självövervakning av blodglukos (SMBG) var 7: e dag. Justering av prandial insulindos utfördes enligt värden före måltid med hjälp av en enkel algoritm med inställda doser av snabbverkande insulin. Patienter följde upp besök från sjuksköterskan vid 1 och 3 veckor, 3 och 6 månader och av endokrinologen vid 2, 4 och 7 månader, där kost kontrollerades och dagbok med SMBG-värden granskades för att justera insulindoserna., Antropometriska data (vikt, kroppsmassindex och midjemått) samt behandlings-och biokemiska variabler erhölls vid baslinjen och vid 3 och 6 månader hos alla patienter. Vi kvantifierade insulinbehov och antalet allvarliga hypoglykemi (definierat som att kräva hjälp) genom anamnese och en översyn av patienternas dagböcker.
HbA1c bestämdes genom högpresterande vätskekromatografi (HPLC) (Bio-Rad Laboratories, München, Tyskland), med ett referensområde på 4,6-5,8%., Kolesterol och triglycerider bestämdes genom standardiserade enzymatiska metoder och lipoproteinkolesterol med hög densitet (HDLc) med en direkt metod (Roche Diagnostics, Basel, Schweiz). Lågdensitetslipoproteinkolesterol (LDLc) uppskattades med Friedewald-formeln (om triglyceridnivåerna var
3.39 mmol/L) eller genom ultracentrifugation. Apolipoprotein (Apo) B har fastställts genom en inmunoturbidimetric metod (Tina-quant, Roche Diagnostics) och LDL storlek genom elektrofores (2-16%)., Livskvaliteten mättes med hjälp av ett sjukdomsspecifikt frågeformulär anpassat i Spanien från Diabetes Quality of Life (DCCT) vid baseline och upprepades vid 6 månader efter basal-bolusinsulinbehandling.3,4
data analyserades av det statistiska programmet SPSS 15.0 (SPSS Inc.). Förändringarna i antropometriska variabler, HbA1c, insulinbehov och lipidprofil utvärderades av T av Studenttest. De ansågs vara signifikanta värden på p≤0,05.
resultat
de kliniska egenskaperna vid baseline sammanfattas i Tabell 1., Sjuttioåtta procent av patienterna behandlades med 2 doser NPH eller förblandade insulinpreparat, 11% av patienterna tog orala läkemedel och bedtime insulin (glargin, detemir eller NPH) och de återstående 11% av patienterna använde andra regimer med 3 doser NPH och vanligt insulin. 87% av patienterna hade en HbA1c-koncentration >8% och 51% hade HbA1c>9%. Efter byte till basal bolusbehandling sjönk HbA1c från 9±1,2% till 8,1±1,2% (p
0,001) vid 3 månader och till 8,0±1,2% vid 6 månader (P0.001) (Tabell 1, Fig. 1)., Andelen patienter med HbA1c≥9% minskade från en initial 51% (19 patienter) till 13, 8% respektive 18, 9%, vid 3 respektive 6 månader. Fig. 2 visar andelen patienter med hba1c7%, 7-8% och>8% före och efter byte till basal-bolusbehandling. Fem av patienterna visade en försämring av HbA1c-värdena. Det fanns bara en episod av allvarlig hypoglykemi registrerad. Vid 6 månader kunde alla patienter justera basinsulindosen, men endast 10 patienter ändrade prandialdosen beroende på mönstret för SMBG autonomt.,
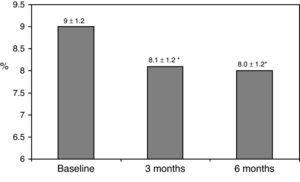
Glycated hemoglobin at baseline and 3 and 6 months after switching to basal-bolus regimen. *p0.001 compared to baseline. HbA1c: glycated hemoglobin.
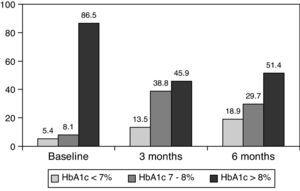
Percentage of patients with glycated hemoglobin 8% at baseline, and 3 and 6 months after switching to basal-bolus regimen.
kroppsvikt, insulinbehov och lipidparametrar vid baslinjen och under uppföljningen visas i Tabell 1. Kroppsvikt förblev stabil under 6 månaders uppföljning och insulinbehovet (UI/kg/dag) förändrades inte vid 3 månader och ökade något vid 6 månader. Storleken på LDL-partiklarna ökade signifikant vid 3 (25,77±0,48 nm vs 25,98±0,5 nm, P0. 05) och 6 månader (25,77±0,48 nm vs 25,94±0,44 nm, P0.05), medan de andra lipidparametrarna inte förändrades.,
diskussion
i denna studie visade vi att basal-bolusinsulinterapi möjliggör glykemisk kontroll för att förbättra utan att äventyra säkerheten och livskvaliteten hos personer med långvarig typ 2-diabetes, som tidigare behandlats med en eller flera insulindoser. Vi visar också genomförbarheten av genomförandet av dessa insulinregimer genom ett strukturerat outpatient träningsprogram.,
Konsensusriktlinjer för hantering av typ 2-diabetes anser att de primära målen för behandlingen är att uppnå HbA1c-koncentrationer så låga som möjligt utan att orsaka oacceptabel hypoglykemi, särskilt hos äldre patienter eller med kranskärlssjukdom, och för att förhindra utvecklingen av mikrovaskulära och makrovaskulära komplikationer.1,5 tyvärr visar de senaste undersökningarna att en stor andel patienter med diabetes inte uppfyller de rekommenderade glykemiska målen.,6,7 Även i National Health and Nutrition Examination Survey (NHANES) andel patienter med HbA1c
7% ökat från 37% 1999-2000 till 56,8 procent under 2003-2004 priser för optimal glykemisk kontroll är särskilt hög för personer med liknande egenskaper som de som studerats av oss, som har långvarig diabetes eller insulinbehandling.,6,7 två gånger dagligen dosering med NPH eller förblandat insulin används för att förenkla insulinregimer, men har begränsad flexibilitet, kräver styv vidhäftning till regelbundna måltider, begränsa förmågan att justera doserna av de enskilda komponenterna och öka risken för hypoglykemi. Således, även om många patienter initialt kommer att uppnå adekvat glykemisk kontroll med denna regim, 8 när insulinsekretorisk kapacitet av betaceller förloras och insulinbrist är svår, blir glykemisk kontroll dålig och instabil som hos de flesta patienter som ingår i denna studie.,18 Vi visade att basal-bolusinsulinregimen hos patienter med långvarig typ 2-diabetes, dåligt kontrollerade med andra insulinregimer och instabil profil, minskar HbA1c en poäng över 6 månader och andelen patienter med HbA1c≥9% från 51% till 14% vid 3 månader och 19% vid 6 månader. Detta beror förmodligen på att det är en mer fysiologisk terapi; medan prandial insulin ersätter endogen insulinsekretion i första fasen, minskar basinsulin nivån av fastande hyperglykemi., Således, förutom nivån av HbA1c 9, förändrar det sätt på vilket behandlingen intensifieras kraftigt de relativa bidragen av basal och postprandial hyperglykemi till den totala hyperglykemi hos T2DM-patienter. Nyligen Gåta et al.10 visade att efter behandling intensifiering med insulin sjunker bidraget från basal hyperglykemi men står fortfarande för ungefär en tredjedel av den kvarvarande hyperglykemi. Därför, enligt resultaten av denna studie, är det ofta nödvändigt att använda insulinregimer som kombinerar basal med prandial insulin för att uppnå glykemiska mål., Faktum är att dessa fynd överensstämmer med de stora bevisen för fördelarna med basal-bolusbehandling vid typ 1-diabetes 11 och stöds av begränsade data från observationsstudier på patienter med typ 2-diabetes som byter från premix till basal-bolus glarginbaserad behandling 12, 13 och genom en randomiserad jämförelse av en premixbaserad behandling jämfört med en basal-bolusbehandling hos patienter med typ 2-diabetes.2,14,15 hos patienter som tidigare behandlats med glargin plus orala anti-diabetiska läkemedel var skillnaden i HbA1c 0.,22% till förmån för basal-bolus glarginbaserad behandling, jämfört med en förblandad insulinregimen15. I PREFER-studien visade 14 undergruppen av patienter som tidigare hade basinsulinbehandling en större HbA1c-reduktion med detemir / aspart basal-bolusregimen jämfört med bifasiskt insulin aspart (- 1, 21% vs-0, 75%). Slutligen, i premixbehandlade typ 2-diabetespatienter, Fritsche et al. visade att en basal-bolus glargin – /glulisinbaserad insulinbehandling var överlägsen en premixinsulin-behandling för att minska HbA1c (- 1, 31% mot 0, 8%).,2 även om det finns skillnader i storleken på förbättringen mellan studierna, troligen på grund av de olika baslinjeegenskaperna hos den studerade populationen, verkar överlägsenheten av en basal-bolusregim hos utvalda patienter med långvarig sjukdom påvisad. Minskningen på mer än en poäng av HbA1c som uppnås genom övergång till en basal-bolusinsulinbehandling kan anses vara kliniskt signifikant eftersom den kan leda till en minskning av kliniska resultat., Tyvärr är basal-bolusbehandling underutnyttjad hos patienter med T2DM eftersom läkare anser att det är komplicerat att genomföra, det är tidskrävande och det finns rädsla för det ökade antalet injektioner, risk för hypoglykemi, viktökning och försämrad livskvalitet. I detta och tidigare studier kroppsvikt och graden av svår hypoglykemi inte ökade,2, 12 som kan relateras till den mer fysiologiska insulin substitution med basal-bolus regim och den flexibilitet som denna behandling kan erbjuda till patienter., Således bör rädsla för hypoglykemi inte vara ett hinder för att starta denna typ av behandling i T2DM, men det måste övervägas för att fastställa glykemiska kontrollmål eftersom det kan orsaka sjuklighet och ökad dödlighet.16 när det gäller inverkan på livskvaliteten, i överensstämmelse med rapporten från Ménard et al., 17 vår studie stödde inte uppfattningen att basal-bolusregimer leder till minskad livskvalitet.
enligt en tidigare rapport kunde 12 i denna studie alla patienter titrera sin basala insulindos enligt den fasta SMBG de senaste 3-7 dagarna., Däremot kunde få patienter justera prandial insulindoser enligt SMBG-mönstren och behövde mest stöd av en enkel algoritm med inställd dos beroende på premeal blodglukos. Detta är inte förvånande eftersom fastställandet av den optimala måltid insulindos innebär ofta beräkningar som anser flera faktorer och är svårt för vissa patienter. Dessutom är det lika effektivt att använda en enkel algoritm för att justera måltid snabbverkande insulin varje vecka baserat på SMBG-mönster som att justera måltid insulin med hjälp av insulin-till-kolhydratförhållanden hos T2DM-personer.,18
Begränsningar av studien är relaterade till den potentiella observationsdesignen och bristen på kontrollgrupp. Dessa aspekter och den korta uppföljningen av patienter, svårt att tolka resultaten och deras tillämplighet på patienter med T2DM följt i andra centra. Även om framtida studier i större grupper av patienter bör utföras för att bekräfta dessa fynd, ger studien information som kan vara användbar för hanteringen av en vanlig och dåligt behandlad klinisk situation.,
Sammanfattningsvis visade den nuvarande studien att ett 9-timmars outpatientprogram gjorde det möjligt för T2DM-patienter med lång varaktighet att dåligt kontrollera med andra insulinregimer att byta till basal-bolusinsulin. Vi bekräftade också att basal-bolusinsulinregimen är effektiv, säker och inte förändrar livskvaliteten hos denna undergrupp av T2DM-patienter. Basal-bolusbehandling kan därför erbjudas patienter med otillräcklig kontroll av T2DM med andra insulinstrategier.
intressekonflikt
Irene Vinagre har fått föreläsning avgifter från Eli Lilly, Novo Nordisk och Sanofi Aventis., Antonio Perez har fått con sulting och föreläsning avgifter från Eli Lilly, Novo Nordisk och Sanofi Aventis.