Introducere
diabet zaharat de Tip 2 (dz de tip 2) este caracterizat de o rezistenta la insulina, care rămâne relativ stabilă în cursul bolii, și o pierdere progresiva a celulelor β funcție cu un inadecvate secreția de insulină., Datorită acestei evoluții progresive, majoritatea pacienților cu T2DM vor necesita în cele din urmă insulină pentru a obține și menține controlul glicemic, folosind o abordare treptată începând cu insulina bazală combinată cu agenți orali. Atunci când glicemia pre-prandială și postprandială nu este controlată în mod adecvat, se preferă un regim de insulină de două ori pe zi cu NPH (protamină neutră Hagedorn) sau preparate de insulină premixate ca pas următor., Ca și la subiecții diabetici de tip 1, terapia cu insulină bazală-bolus trebuie indicată la pacienții cu deficit sever de insulină T2DM care nu pot atinge și menține țintele glicemice cu regim de două ori pe zi.1 Cu toate acestea, acest regim de insulină este în mod clar insuficient utilizat, probabil din cauza reticenței pacienților și a Medicilor din cauza complexității implicate în stabilirea sa, precum și a informațiilor limitate disponibile despre fezabilitate, în special la subiecții vârstnici, și eficacitatea sa la pacienții tratați anterior cu două doze de insulină.,2
în studiul de față, am evaluat fezabilitatea, eficacitatea și siguranța terapiei cu insulină bazală-bolus la pacienții cu diabet zaharat de tip 2 pe termen lung și control glicemic slab sau instabil.Material și metode în acest studiu prospectiv, unicentric, am înrolat 37 de pacienți care au trecut la regimul insulin bazal-bolus din octombrie 2006 până în octombrie 2007 și au avut un control glicemic instabil sau slab (hemoglobină glicată (HbA1c)≥8%) în primele șase luni, în ciuda intervenției de îmbunătățire a acestuia., Protocolul studiului a fost aprobat de comisiile instituționale de evaluare etică și a fost obținut consimțământul scris în cunoștință de cauză de la toți pacienții.în tratamentul inițial, carbohidrații au fost Distribuiți pe parcursul celor trei mese principale. Doza inițială de insulină glargin a fost calculată ca 50% din doza zilnică totală anterioară, iar insulina prandială inițială (aspart sau lispro) ca restul de 50% din doza zilnică totală, care a fost împărțită în mod egal pentru a acoperi cele trei mese., Pacienții care au luat metformină înainte de a schimba tratamentul și nu au avut nicio contraindicație pentru aceasta, au continuat să o utilizeze în aceeași doză. Celelalte medicamente antidiabetice orale au fost oprite.
toți pacienții au participat la un program structurat de instruire în ambulatoriu privind diabetul zaharat, format din trei sesiuni de grup 2-h într-o săptămână, pentru 5-8 pacienți. În general, ei au fost învățați să urmeze o dietă presupunând un aport calitativ de carbohidrați la fiecare masă, deși pentru pacienții care doreau să o modifice, trebuia făcută numărarea carbohidraților., Pacienții au învățat, de asemenea, gestionarea terapiei bazal-bolus și modul de ajustare a dozelor de insulină bazală în funcție de auto-monitorizarea glicemiei (SMBG) la fiecare 7 zile. Ajustarea dozei de insulină prandială a fost efectuată în funcție de valorile pre-masă utilizând un algoritm simplu cu doze stabilite de insulină cu acțiune rapidă. Pacienții au urmărit vizitele furnizate de asistentă la 1 și 3 săptămâni, 3 și 6 luni și de endocrinolog la 2, 4 și 7 luni, unde a fost verificată dieta și a fost revizuit jurnalul cu valorile SMBG pentru ajustarea dozelor de insulină., Datele antropometrice (greutatea, indicele de masă corporală și circumferința taliei), precum și variabilele de tratament și biochimice au fost obținute la momentul inițial și la 3 și 6 luni la toți pacienții. Am cuantificat necesarul de insulină și numărul de hipoglicemii severe (definite ca necesitând asistență) prin anamneză și o revizuire a jurnalelor pacienților.
HbA1c a fost determinat prin cromatografie lichidă de înaltă performanță (HPLC) (Bio-Rad Laboratories, Munchen, Germania), cu un interval de referință de 4,6–5,8%., Colesterolul și trigliceridele au fost determinate prin metode enzimatice standardizate și colesterol lipoproteic cu densitate mare (HDLc) printr-o metodă directă (Roche Diagnostics, Basel, Elveția). Colesterolul lipoproteinelor cu densitate scăzută (LDLc) a fost estimat prin formula Friedewald (dacă nivelurile de trigliceride au fost
3, 39 mmol/l) sau prin ultracentrifugare. Apolipoproteina (Apo) B a fost determinată printr-o metodă inmunoturbidimetrică (Tina-quant, Roche Diagnostics) și mărimea LDL prin electroforeză (2-16%)., Calitatea vieții a fost măsurată utilizând un chestionar specific bolii adaptat în Spania din studiul privind calitatea vieții diabetului (DCCT) la momentul inițial și repetat la 6 luni după tratamentul cu insulină bazal-bolus.Datele 3,4
au fost analizate de programul statistic SPSS 15.0 (SPSS Inc.). Modificările variabilelor antropometrice, HbA1c, necesităților de insulină și profilului lipidic au fost evaluate prin testul T al studenților. Au fost considerate valori semnificative de p≤0,05.
rezultate
caracteristicile clinice inițiale sunt rezumate în tabelul 1., Șaptezeci și opt la sută dintre pacienți au fost tratați cu 2 doze de NPH sau preparate de insulină premixate, 11% dintre pacienți au luat medicamente orale și insulină de culcare (glargin, detemir sau NPH), iar restul de 11% dintre pacienți au utilizat alte regimuri cu 3 doze de NPH și insulină regulată. -Optzeci și șapte la sută dintre pacienți au avut un concentrația de HbA1c >8% și 51% au avut valori ale HbA1c>9%. După trecerea la bazal-bolus, HbA1c a scăzut de la 9±1.2% la 8,1±1.2% (p
0.001), la 3 luni și la 8,0±1.2% la 6 luni (p0.001) (Tabelul 1, Fig. 1)., Procentul de pacienți cu HbA1c≥9% a scăzut de la un număr inițial de 51% (19 subiecți) la 13, 8% și 18, 9%, la 3 și, respectiv, 6 luni. Fig. 2 arată proporția de pacienți cu o HbA1c7%, 7-8% și >8% înainte și după trecerea la bazal-bolus. Cinci dintre pacienți au prezentat o agravare a valorilor HbA1c. A fost înregistrat un singur episod de hipoglicemie severă. La 6 luni, toți pacienții au putut ajusta doza bazală de insulină, dar numai 10 pacienți au modificat doza prandială în funcție de modelele SMBG în mod autonom.,
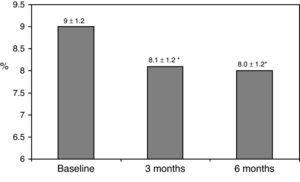
Glycated hemoglobin at baseline and 3 and 6 months after switching to basal-bolus regimen. *p0.001 compared to baseline. HbA1c: glycated hemoglobin.
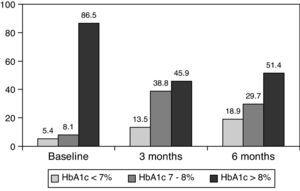
Percentage of patients with glycated hemoglobin 8% at baseline, and 3 and 6 months after switching to basal-bolus regimen.
greutate corporala, necesarul de insulină și parametrilor lipidici la momentul inițial și în timpul follow-up sunt prezentate în Tabelul 1. Greutatea corporală a rămas stabilă pe parcursul celor 6 luni de urmărire, iar necesarul de insulină (UI/kg și zi) nu s-a modificat la 3 luni și a crescut ușor la 6 luni. Dimensiunea de particule LDL crescut semnificativ de la 3 (25.77±0.48 nm vs 25.98±0.5 nm, p0.05) și 6 luni (25.77±0.48 nm vs 25.94±0.44 nm, p0.05), în timp ce alte lipidic parametri nu se schimba.,în studiul de față, am arătat că terapia cu insulină bazală-bolus permite îmbunătățirea controlului glicemic fără a compromite securitatea și calitatea vieții la subiecții cu diabet zaharat de tip 2 pe termen lung, tratați anterior cu una sau mai multe doze de insulină. De asemenea, demonstrăm fezabilitatea implementării acestor regimuri de insulină printr-un program structurat de instruire în ambulatoriu.,Ghidul consensului pentru gestionarea diabetului de tip 2 consideră că obiectivele principale ale tratamentului sunt atingerea concentrațiilor de HbA1c cât mai scăzute posibil, fără a provoca hipoglicemie inacceptabilă, în special la pacienții vârstnici sau cu boală coronariană și pentru a preveni dezvoltarea complicațiilor microvasculare și macrovasculare.1,5 din păcate, studiile recente indică faptul că o mare parte din pacienții cu diabet zaharat nu reușesc să îndeplinească obiectivele glicemice recomandate.,6,7 Deși în National de Sanatate si Nutritie Ancheta de Examinare (NHANES) proporția de pacienți cu HbA1c
7% a crescut de la 37% în 1999-2000 la 56,8% în 2003-2004, ratele de control glicemic suboptimal sunt deosebit de bogate în indivizi cu caracteristici similare celor studiate de noi, care au o lungă durată de diabet sau de tratament cu insulină.,6,7 administrarea de două ori pe zi cu insulină NPH sau preamestecată este utilizată pentru a simplifica regimurile de insulină, dar au o flexibilitate limitată, necesită respectarea rigidă a meselor regulate, limitează capacitatea de ajustare a dozelor componentelor individuale și crește posibilitatea hipoglicemiei. Astfel,deși mulți pacienți vor obține inițial un control glicemic adecvat cu acest regim 8, când capacitatea secretorie de insulină a celulelor beta este pierdută și deficitul de insulină este sever, controlul glicemic devine slab și instabil ca la majoritatea pacienților incluși în studiul de față.,1,8 am arătat că la pacienții cu diabet zaharat de tip 2 pe termen lung, slab controlat cu alte regimuri de insulină și profil instabil, regimul de insulină bazal-bolus reduce HbA1c cu un punct peste 6 luni și proporția pacienților cu HbA1c≥9% de la 51% la 14% la 3 luni și 19% la 6 luni. Acest lucru se datorează probabil faptului că este o terapie mai fiziologică; în timp ce insulina prandială înlocuiește secreția de insulină endogenă de primă fază, insulina bazală scade nivelul hiperglicemiei în repaus., Astfel, în plus față de nivelul HbA1c 9, modul în care tratamentul este intensificat modifică foarte mult contribuțiile relative ale hiperglicemiei bazale și postprandiale la hiperglicemia globală a pacienților cu T2DM. Recent, Riddle și colab.10 a arătat că, după intensificarea tratamentului cu insulină, contribuția hiperglicemiei bazale scade, dar reprezintă încă aproximativ o treime din hiperglicemia rămasă. Prin urmare, conform rezultatelor studiului de față, utilizarea regimurilor de insulină care combină insulina bazală cu insulina prandială va fi adesea necesară pentru atingerea obiectivelor glicemice., În fapt, aceste constatări sunt în concordanță cu vasta dovezi pentru avantajele bazal-bolus, în diabet zaharat de tip 1 11 și sunt susținute de date limitate din studiile observaționale la pacienții cu diabet zaharat de tip 2 trecerea de la premix pentru basal-bolus glargin regim pe bază de 12,13 și de un studiu randomizat de comparare a unui premix pe baza de față de un regim bazal-bolus regim de tip 2, la pacienții cu diabet zaharat.2,14,15 la pacienții tratați anterior cu glargin plus medicamente antidiabetice orale, diferența de HbA1c a fost 0.,22% în favoarea regimului bazal-bolus pe bază de glargin, comparativ cu un regim de insulină premixat15. În PREFERA studiu,14 subgrupul de pacienți anterior pe o insulină bazală regim arătat o mai mare de reducere a HbA1c cu detemir/aspart basal-bolus regim comparativ cu bifazică de insulină aspart (-1.21% vs -0.75%). În cele din urmă, la pacienții diabetici de tip 2 tratați cu premix, Fritsche et al. a demonstrat că un regim de insulină bazal-bolus glargin/glulizină a fost superior unui regim de insulină premix în reducerea HbA1c (-1, 31% față de 0, 8%).,2 Prin urmare, deși există diferențe în ceea ce privește amploarea ameliorării între studii, probabil datorită caracteristicilor inițiale diferite ale populației studiate, superioritatea unui regim bazal-bolus la pacienții selectați cu boală de lungă durată pare demonstrată. Reducerea a mai mult de un punct de HbA1c obținută prin trecerea la o schemă de tratament cu insulină bazală-bolus poate fi considerată semnificativă din punct de vedere clinic, deoarece poate duce la reducerea rezultatelor clinice., Din păcate, terapia bazală-bolus este subutilizată la pacienții cu T2DM, deoarece medicii consideră că este complexă de implementat, consumă mult timp și există temeri legate de numărul crescut de injecții, riscul de hipoglicemie, creșterea în greutate și agravarea calității vieții. În acest studiu și în studiile anterioare, greutatea corporală și rata hipoglicemiei severe nu au crescut,2,12, ceea ce ar putea fi legat de substituția fiziologică a insulinei cu regimul bazal-bolus și de flexibilitatea pe care această terapie o poate oferi pacienților., Astfel, frica de hipoglicemie nu ar trebui să fie o barieră pentru a începe acest tip de terapie în T2DM, dar trebuie luată în considerare pentru a stabili obiective de control glicemic, deoarece poate provoca morbiditate și mortalitate crescută.16 în ceea ce privește impactul asupra calității vieții, în concordanță cu raportul Ménard et al., 17 studiul nostru nu a susținut opinia că regimurile bazal-bolus duc la o scădere a calității vieții.
conform unui raport anterior, 12 în studiul de față, toți pacienții au putut să-și titreze doza bazală de insulină în funcție de SMBG de repaus alimentar din ultimele 3-7 zile., În schimb, puțini pacienți au fost capabili să ajusteze dozele de insulină prandială în funcție de tiparele SMBG și au avut nevoie de sprijinul unui algoritm simplu cu doză stabilită în funcție de glicemia premeală. Acest lucru nu este surprinzător, deoarece stabilirea dozei optime de insulină la masă implică adesea calcule care iau în considerare mai mulți factori și este dificil pentru unii pacienți. Mai mult, utilizarea unui algoritm simplu pentru ajustarea insulinei cu acțiune rapidă în fiecare săptămână pe baza modelelor SMBG este la fel de eficientă ca ajustarea insulinei la masă folosind rapoarte insulină-carbohidrați la subiecții T2DM.,18
Limitările studiului sunt legate de proiectarea observațională prospectivă și de lipsa grupului de control. Aceste aspecte și urmărirea scurtă a pacienților, dificil de interpretat constatările și aplicabilitatea lor la pacienții cu T2DM urmăriți în alte centre. Cu toate acestea, deși studiile viitoare pe grupuri mai mari de pacienți ar trebui efectuate pentru a confirma aceste constatări, studiul oferă informații care pot fi utile pentru gestionarea unei situații clinice comune și slab tratate.,
În concluzie, studiul de față a demonstrat că un program de 9 ore în ambulatoriu a permis pacienților cu T2DM de lungă durată, slab controlați cu alte regimuri de insulină, să treacă la regimul de insulină bazal-bolus. De asemenea, am confirmat că regimul de insulină bazal-bolus este eficient, sigur și nu modifică calitatea vieții în acest subgrup de pacienți cu T2DM. Astfel, terapia bazală-bolus ar putea fi oferită subiecților T2DM controlați inadecvat cu alte strategii de insulină.
Conflict de interese
Irene Vinagre a primit taxe de curs de la Eli Lilly, Novo Nordisk și Sanofi Aventis., Antonio Perez a primit taxe de con sulting și curs de la Eli Lilly, Novo Nordisk și Sanofi Aventis.