Inleiding
Type 2 diabetes mellitus (T2DM) wordt gekenmerkt door een insulineresistentie, die gedurende het verloop van de ziekte relatief stabiel blijft, en een progressief verlies van β-celfunctie met een inadequate insulinesecretie., Wegens deze progressieve evolutie, zullen de meeste patiënten met T2DM uiteindelijk insuline vereisen om glycemische controle te bereiken en te handhaven, gebruikend een stapsgewijze benadering beginnend met basale insuline die met mondelinge agenten wordt gecombineerd. Wanneer preprandiale en postprandiale glycemie niet voldoende onder controle is, wordt als volgende stap de voorkeur gegeven aan een tweemaal daags insulineschema met NPH (Neutral Protamine Hagedorn) of voorgemengde insulinepreparaten., Net als bij type 1 diabetespatiënten, dient basale bolusinsulinetherapie geïndiceerd te zijn bij T2DM-patiënten met ernstige insulinetekort die niet in staat zijn glycemische doelen te bereiken en te handhaven met een tweemaal daags regime.1 Dit insulineregime wordt echter duidelijk onderbenut, waarschijnlijk vanwege de terughoudendheid van patiënten en artsen als gevolg van de complexiteit die betrokken is bij de oprichting ervan, evenals de beperkte informatie die beschikbaar is over de haalbaarheid, met name bij oudere proefpersonen, en de werkzaamheid bij patiënten die eerder met twee insulinedoses werden behandeld.,2
in deze studie hebben we de haalbaarheid, effectiviteit en veiligheid van basaal-bolus insulinetherapie geëvalueerd bij patiënten met langdurige type 2 diabetes en slechte of instabiele glycemische controle.
materiaal en methoden
in deze prospectieve, single-centerstudie namen we 37 patiënten in die van oktober 2006 tot oktober 2007 overschakelden op basaal-bolusinsulineregime en die in de voorafgaande zes maanden een instabiele of slechte glycemische controle (geglyceerd hemoglobine (HbA1c)≥8%) hadden gehad, ondanks interventie om het te verbeteren., Het onderzoeksprotocol werd goedgekeurd door de institutional ethics review boards en van alle patiënten werd geïnformeerde schriftelijke toestemming verkregen.
tijdens de initiële behandeling werden koolhydraten verdeeld over de drie hoofdmaaltijden. De aanvangsdosis insuline glargine werd berekend als 50% van de voorgaande totale dagdosering en de aanvangsdosis prandiale insuline (aspart of lispro) als de resterende 50% van de totale dagdosering, die gelijkelijk verdeeld was over de drie maaltijden., Patiënten die metformine gebruikten voordat zij overschakelden en die geen contra-indicatie hadden, bleven het middel gebruiken in dezelfde dosis. De andere orale antidiabetica werden gestopt.
alle patiënten woonden een gestructureerd poliklinisch diabetestrainingsprogramma bij dat bestond uit drie 2-h-groepsessies in één week voor 5-8 patiënten. In het algemeen werd hen geleerd een dieet te volgen waarbij werd uitgegaan van een kwalitatieve inname van koolhydraten bij elke maaltijd, hoewel voor patiënten die deze wilden variëren, het tellen van koolhydraten moest worden gedaan., Patiënten leerden ook de behandeling van de basaal-bolustherapie en hoe de basale insulinedoses moeten worden aangepast aan de hand van nuchtere zelfcontrole van de bloedglucose (SMBG) om de 7 dagen. Aanpassing van de dosis prandiale insuline werd uitgevoerd volgens de waarden vóór de maaltijd met behulp van een eenvoudig algoritme met vaste doses snelwerkende insuline. Patiënten volgden de bezoeken van de verpleegkundige op 1 en 3 weken, 3 en 6 maanden, en van de endocrinoloog op 2, 4 en 7 maanden, waar het dieet werd gecontroleerd en dagboek met SMBG-waarden werd herzien om de insulinedoses aan te passen., Antropometrische gegevens (gewicht, body mass index en tailleomtrek) evenals behandelingsvariabelen en biochemische variabelen werden verkregen bij aanvang en na 3 en 6 maanden bij alle patiënten. We gekwantificeerd insulinebehoefte en het aantal ernstige hypoglykemie (gedefinieerd als hulp nodig) door anamnese en een herziening van de dagboeken van de patiënten.
HbA1c werd bepaald met behulp van hogedrukvloeistofchromatografie (HPLC) (Bio-Rad Laboratories, München, Duitsland), met een referentiebereik van 4,6-5,8%., Cholesterol en triglyceriden werden bepaald door gestandaardiseerde enzymatische methoden en high-density lipoproteïne cholesterol (HDLc) door een directe methode (Roche Diagnostics, Bazel, Zwitserland). Low-density lipoproteïne-cholesterol (LDLc) werd geschat met de Friedewald-formule (als de triglyceridenspiegels
3,39 mmol/l waren) of door ultracentrifugatie. Apolipoproteïne (Apo) B werd bepaald met een inmunoturbidimetrische methode (Tina-quant, Roche diagnostiek) en LDL grootte door elektroforese (2-16%)., De kwaliteit van leven werd gemeten aan de hand van een ziektespecifieke vragenlijst die in Spanje werd aangepast aan de Diabetes Quality of Life (DCCT) bij baseline en die 6 maanden na basale bolusinsulinetherapie werd herhaald.3,4
gegevens werden geanalyseerd door het statistisch programma SPSS 15.0 (SPSS Inc.). De veranderingen in antropometrische variabelen, HbA1c, insulinebehoefte en lipidenprofiel werden geëvalueerd door T van Student test. Ze werden beschouwd als significante waarden van p≤0,05.
resultaten
de klinische kenmerken bij baseline zijn samengevat in Tabel 1., Achtenzeventig procent van de patiënten werd behandeld met 2 doses NPH of voorgemengde insulinepreparaten, 11% van de patiënten nam orale geneesmiddelen en insuline voor het slapen gaan (glargine, detemir of NPH) en de overige 11% van de patiënten gebruikte andere regimes met 3 doses NPH en kortwerkende insuline. Zevenentachtig procent van de patiënten had een HbA1c-concentratie >8% en 51% had HbA1c>9%. Na overschakeling op basaal-bolustherapie daalde het HbA1c van 9±1,2% tot 8,1±1,2% (p
0,001) na 3 maanden en tot 8,0±1,2% na 6 maanden (p0.001) (Tabel 1, Fig. 1)., Het percentage patiënten met HbA1c≥9% daalde van een initiële 51% (19 proefpersonen) naar 13,8% en 18,9%, respectievelijk na 3 en 6 maanden. Fig. 2 toont het percentage patiënten met een HbA1c7%, 7-8% en >8% voor en na het overschakelen op basaal-bolustherapie. Vijf van de patiënten vertoonden een verslechtering van de HbA1c-waarden. Er was slechts één episode van ernstige hypoglykemie geregistreerd. Na 6 maanden waren alle patiënten in staat om de basale insulinedosis aan te passen, maar slechts 10 patiënten pasten de prandiale dosis aan volgens de patronen van SMBG autonoom.,
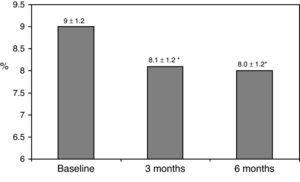
Glycated hemoglobin at baseline and 3 and 6 months after switching to basal-bolus regimen. *p0.001 compared to baseline. HbA1c: glycated hemoglobin.
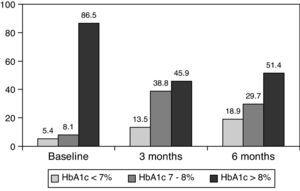
Percentage of patients with glycated hemoglobin 8% at baseline, and 3 and 6 months after switching to basal-bolus regimen.
lichaamsgewicht, insulinebehoefte en lipideparameters bij aanvang en tijdens de follow-up zijn weergegeven in Tabel 1. Het lichaamsgewicht bleef stabiel gedurende de 6 maanden van de follow-up en de insulinebehoefte (UI/kg/dag) veranderde na 3 maanden niet en nam na 6 maanden licht toe. De grootte van de LDL-deeltjes nam significant toe bij 3 (25,77±0,48 nm vs 25,98±0,5 nm, p0.05) en 6 maanden (25,77±0,48 nm vs 25,94±0,44 nm, p0.05), terwijl de andere lipidenparameters niet veranderden.,
discussie
in deze studie hebben we aangetoond dat basaal-bolus insulinetherapie de glycemische controle kan verbeteren zonder de veiligheid en kwaliteit van leven in gevaar te brengen bij personen met langdurige type 2 diabetes, die eerder behandeld werden met één of meer insulinedoses. We demonstreren ook de haalbaarheid van de implementatie van deze insulineregimes door middel van een gestructureerd poliklinisch trainingsprogramma.,
Consensusrichtlijnen voor de behandeling van type 2 diabetes zijn van mening dat de primaire doelen van de behandeling zijn om zo laag mogelijk HbA1c-concentraties te bereiken zonder onaanvaardbare hypoglykemie te veroorzaken, vooral bij oudere patiënten of met coronaire aandoeningen, en om de ontwikkeling van microvasculaire en macrovasculaire complicaties te voorkomen.1,5 helaas blijkt uit recente onderzoeken dat een groot deel van de patiënten met diabetes niet voldoet aan de aanbevolen glycemische doelstellingen.,6,7 hoewel in de National Health and Nutrition Examination Survey (NHANES) het percentage patiënten met HbA1c
7% steeg van 37% in 1999-2000 tot 56,8% in 2003-2004, zijn de percentages van suboptimale glycemische controle vooral hoog bij personen met vergelijkbare kenmerken als die welke door ons zijn bestudeerd, die al lang diabetes of insulinebehandeling hebben.,6,7 tweemaal daags doseren met NPH of voorgemengde insuline wordt gebruikt om insulineregimes te vereenvoudigen, maar heeft beperkte flexibiliteit, vereist rigide naleving van regelmatige maaltijden, beperkt het vermogen om de doseringen van de individuele componenten aan te passen en verhoogt de kans op hypoglykemie. Hoewel veel patiënten aanvankelijk voldoende glucosecontrole zullen bereiken met dit regime,8 wanneer de insulinesecretorische capaciteit van bètacellen verloren gaat en de insulinetekort ernstig is, wordt de glucosecontrole slecht en instabiel, zoals bij de meeste patiënten die in dit onderzoek zijn opgenomen.,We toonden aan dat bij patiënten met type 2 diabetes op lange termijn, die slecht onder controle waren met andere insulineregimes en instabiel profiel, het basaal-bolus insulineregime het HbA1c één punt verlaagt gedurende 6 maanden en het percentage patiënten met HbA1c≥9% van 51% naar 14% na 3 maanden en 19% na 6 maanden. Dit is waarschijnlijk omdat het een meer fysiologische therapie is; terwijl prandiale insuline de eerste fase endogene insulinesecretie vervangt, vermindert basale insuline het niveau van nuchtere hyperglycemie., Aldus, naast het niveau van HbA1c 9 verandert de manier behandeling wordt geïntensiveerd sterk de relatieve bijdragen van basale en postprandiale hyperglycemie aan de Algemene hyperglycemie van patiënten T2DM. Onlangs, Riddle et al.10 toonde aan dat na intensivering van de behandeling met insuline, de bijdrage van basale hyperglycemie daalt, maar nog steeds goed is voor ongeveer een derde van de resterende hyperglycemie. Daarom zal, volgens de bevindingen van deze studie, het gebruik van insulineregimes die basaal met prandiale insuline combineren vaak nodig zijn om glycemische doelen te bereiken., In feite zijn deze bevindingen consistent met het uitgebreide bewijs voor de voordelen van basaal-bolustherapie bij type 1-diabetes 11 en worden ondersteund door de beperkte gegevens uit observationele studies bij patiënten met type 2-diabetes die overstappen van premix op basaal-bolus glargine-gebaseerd regime 12,13 en door een gerandomiseerde vergelijking van een premix-gebaseerd regime versus een basaal-bolusregime bij type 2-diabetespatiënten.2,14,15 bij patiënten die eerder behandeld werden met glargine plus orale antidiabetica was het verschil in HbA1c 0.,22% voor de basaal-bolus glargine-gebaseerde behandeling, vergeleken met een voorgemengde insulineregime 15. In de PREFER-studie 14 toonde de subgroep van patiënten die eerder een basaal insulineregime kregen een grotere HbA1c-reductie met het basaal-bolusregime detemir/aspart vergeleken met bifasische insuline aspart (-1,21% vs -0,75%). Tot slot, bij met premix behandelde type 2 diabetespatiënten, Fritsche et al. toonde aan dat een basaal-bolus insulinebehandeling op basis van glargine/glulisine superieur was aan een premix insulinebehandeling wat betreft de verlaging van HbA1c (-1,31% Versus 0,8%).,2 daarom lijkt de superioriteit van een basaal-bolusregime bij geselecteerde patiënten met een langdurige ziekte aangetoond, hoewel er verschillen zijn in de mate van verbetering tussen de onderzoeken, waarschijnlijk als gevolg van de verschillende uitgangskenmerken van de onderzochte populatie. De reductie van meer dan één punt van HbA1c die wordt bereikt door over te schakelen op een basaal-bolusinsulineregime kan als klinisch significant worden beschouwd omdat dit kan resulteren in de reductie van klinische resultaten., Helaas, wordt de basaal-bolustherapie onderbenut in patiënten met T2DM omdat de artsen het complex beschouwen om uit te voeren, het tijdrovend is en er angsten van het verhoogde aantal injecties, risico van hypoglykemie, gewichtsaanwinst en het verslechteren kwaliteit van leven zijn. In deze en eerdere studies waren het lichaamsgewicht en de snelheid van ernstige hypoglykemie niet verhoogd,2,12, wat gerelateerd kan zijn aan de meer fysiologische insulinesubstitutie met basaal-bolus regime en de flexibiliteit die deze therapie kan bieden aan patiënten., Aldus, zou de angst voor hypoglykemie geen barrière moeten zijn om dit soort therapie in T2DM te beginnen, maar het moet worden overwogen om glycemische controledoelstellingen vast te stellen aangezien het morbiditeit en verhoogde mortaliteit kan veroorzaken.16 met betrekking tot de impact op de kwaliteit van het leven, in overeenstemming met het rapport van Ménard et al., 17 onze studie onderbouwde niet de opvatting dat basale-bolusregimes leiden tot een verminderde kwaliteit van leven.
volgens een eerder rapport 12 waren in dit onderzoek alle patiënten in staat hun basale insulinedosis te titreren volgens het nuchtere SMBG van de laatste 3-7 dagen., Weinig patiënten daarentegen waren in staat om de prandiale insulinedoses aan te passen aan de patronen van SMBG en hadden de ondersteuning van een eenvoudig algoritme met een ingestelde dosis afhankelijk van de bloedglucose voor de maaltijd het meest nodig. Dit is niet verwonderlijk, omdat het vaststellen van de optimale maaltijd insuline dosis vaak berekeningen die rekening houden met meerdere factoren en is moeilijk voor sommige patiënten. Bovendien is het gebruik van een eenvoudig algoritme om de snelwerkende insuline per week aan te passen op basis van SMBG-patronen net zo effectief als het aanpassen van de insuline tijdens de maaltijd met behulp van insuline-koolhydraat-verhoudingen bij T2DM-proefpersonen.,18
Beperkingen van het onderzoek houden verband met de prospectieve observationele opzet en het ontbreken van de controlegroep. Deze aspecten en de korte follow-up van patiënten, moeilijk om de bevindingen en hun toepasselijkheid op patiënten met T2DM te interpreteren die in andere centra worden gevolgd. Hoewel toekomstige studies bij grotere groepen patiënten moeten worden uitgevoerd om deze bevindingen te bevestigen, levert het onderzoek informatie op die nuttig kan zijn voor de behandeling van een veel voorkomende en slecht behandelde klinische situatie.,
concluderend, toonde dit onderzoek aan dat een 9-uur durende out-patient programma het mogelijk maakte voor langdurige T2DM patiënten die slecht onder controle waren met andere insuline regimes om over te schakelen op basaal-bolus insuline regime. We hebben ook bevestigd dat basaal-bolus insuline regime effectief, veilig is en de kwaliteit van leven in deze subgroep van T2DM patiënten niet verandert. Aldus basaal-bolustherapie zou aan T2DM onderwerpen kunnen worden aangeboden die onvoldoende met andere insulinestrategieën worden gecontroleerd.Irene Vinagre heeft collegegeld ontvangen van Eli Lilly, Novo Nordisk en Sanofi Aventis., Antonio Perez heeft advies-en collegegeld ontvangen van Eli Lilly, Novo Nordisk en Sanofi Aventis.