Learning Objectives
- staat voor Hund’ s rule.
- Pas de regel van Hund toe op het vullen van orbitalen.
- gebruik orbitale vuldiagrammen om de locaties van elektronen in een atoom te beschrijven.
heeft u zich ooit afgevraagd wat die load limit-tekens op een brug betekenen?
het teken hierboven zegt dat niets meer dan vijf ton is toegestaan omdat het schade aan de structuur zal veroorzaken., Er zijn grenzen aan de hoeveelheid gewicht die een brug kan dragen, er zijn grenzen aan het aantal mensen dat veilig een kamer kan bezetten, en er zijn grenzen aan wat in een elektronenbaan kan gaan.

Hund ‘ s Rule
de laatste van de drie regels voor het construeren van elektronenarrangementen vereist dat elektronen één voor één in een verzameling orbitalen binnen hetzelfde subniveau worden geplaatst. Dit minimaliseert de natuurlijke afstotende krachten die een elektron heeft voor een ander elektron., De regel van Hund stelt dat orbitalen van gelijke energie elk door één elektron worden bezet voordat een orbitaal door een tweede elektron wordt bezet en dat elk van de afzonderlijke elektronen dezelfde spin moet hebben. De figuur hieronder laat zien hoe een verzameling van drie p-orbitalen gevuld is met één, twee, drie en vier elektronen.
orbitale Vuldiagrammen
een orbitale vuldiagram is de meer visuele manier om de opstelling van alle elektronen in een bepaald atoom weer te geven., In een orbitaal vullend diagram worden de individuele orbitalen weergegeven als cirkels (of vierkanten) en orbitalen binnen een subniveau worden horizontaal naast elkaar getekend. Elk subniveau wordt gelabeld door zijn belangrijkste energieniveau en subniveau. Elektronen worden aangegeven door pijlen in de cirkels. Een pijl naar boven wijst de ene spinrichting aan, terwijl een pijl naar beneden de andere richting aangeeft. De orbitale vuldiagrammen voor waterstof, helium en lithium zijn weergegeven in onderstaande figuur.
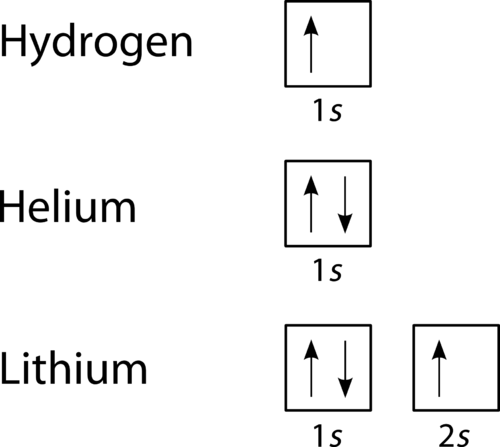
Figuur 2., Orbitale vuldiagrammen voor waterstof, helium en lithium.
volgens het Aufbau-proces worden subniveaus en orbitalen gevuld met elektronen in volgorde van toenemende energie. Aangezien het s-subniveau uit slechts één orbitaal bestaat, paren de tweede elektronen simpelweg met het eerste elektron zoals in helium. Het volgende element is lithium en vereist het gebruik van het volgende beschikbare subniveau, de 2s.
het vuldiagram voor koolstof is weergegeven in de onderstaande figuur. Er zijn twee 2 p elektronen voor koolstof en elk neemt zijn eigen 2 p orbitaal in.,
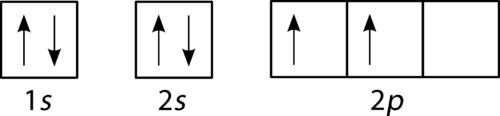
Figuur 3. Orbitaal vulschema voor koolstof.
zuurstof heeft vier 2 p-elektronen. Nadat elke 2 p orbitaal een elektron heeft, kan het vierde elektron in de eerste 2 p orbitaal geplaatst worden met een spin tegenover die van het andere elektron in die orbitaal.
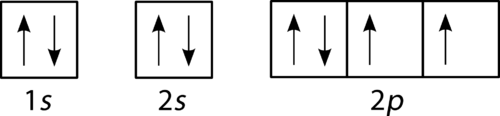
Figuur 4. Orbitaal vulschema voor zuurstof.
samenvatting
- de regel van Hund bepaalt de volgorde van elektronenvulling binnen een verzameling orbitalen.,
- orbitale vuldiagrammen zijn een manier om elektronenlocaties in orbitalen aan te geven.
praktijk
Gebruik de onderstaande link om de volgende oefening uit te voeren:
https://www.caymanchem.com/app/template/chemAssistant,Tool.vm / itemid / 4001
- selecteer een atoom uit de lijst (u wilt waarschijnlijk lagere atoomnummers doen). Laat het getal een nul instellen.
- zoek het atoom op in een periodiek systeem en bepaal het aantal aanwezige elektronen.
- teken het orbitale vuldiagram voor het atoom.,
- klik op de” Bereken ” knop en vergelijk uw antwoord met het gegeven antwoord.
bekijk
- Geef de regel van Hund weer.
- Wat is een orbitaal vuldiagram?
- is het diagram in onderstaande figuur juist? Leg je antwoord uit.

- Is het diagram in onderstaande figuur juist? Leg je antwoord uit.,

verklarende woordenlijst
- Hund ‘ s regel: orbitalen van gelijke energie worden elk bezet door een elektron voordat een orbitaal wordt bezet door een tweede elektron en dat elk van de afzonderlijke elektronen dezelfde spin moet hebben.
- orbitaal vuldiagram: een visuele manier om de rangschikking van alle elektronen in een bepaald atoom weer te geven.