Innledning
Type 2 diabetes mellitus (T2DM) er preget av en insulinresistens, som fortsatt er relativt stabil gjennom hele sykdomsforløpet, og et progressivt tap av β-celle funksjon med en manglende insulinsekresjon., På grunn av dette progressiv evolusjon, de fleste pasienter med T2DM vil til slutt krever insulin for å oppnå og opprettholde glykemisk kontroll, ved hjelp av en stegvis tilnærming som begynner med basal insulin kombinert med orale midler. Når pre-prandial og postprandial glycemia ikke er tilstrekkelig kontrollert, en to ganger daglig insulin diett med NPH (Nøytral Protamine Hagedorn) eller ferdigblandet insulin forberedelser er foretrukket som neste trinn., Som i type 1 diabetiker fag, basal-bolus insulin terapi bør være angitt i T2DM pasienter med alvorlig mangel på insulin som er i stand til å oppnå og opprettholde glykemisk mål med to ganger daglig diett.1 Men dette insulin regime er klart underutnyttet sannsynligvis på grunn av motvilje mot pasienter og leger på grunn av kompleksiteten involvert i etableringen samt begrenset informasjon tilgjengelig om de mulighetene, spesielt i eldre emner, og dens virkning på pasienter som tidligere er behandlet med to doser insulin.,2
I denne undersøkelsen, har vi vurdert muligheten for, effektivitet og sikkerhet av basal-bolus insulin terapi hos pasienter med langvarige, type 2 diabetes og dårlig eller ustabilt glykemisk kontroll.
Materiale og metoder
I denne prospektive, enkelt sentrum studien, vi registrert 37 pasienter som ble slått til basal-bolus insulin diett fra oktober 2006 til oktober 2007, og hadde hatt ustabil eller dårlig glykemisk kontroll (glycated hemoglobin (HbA1c)≥8%) i før seks måneder, til tross for tiltak for å forbedre det., Studien protokollen ble godkjent av den institusjonelle etikk gjennomgang boards og informert skriftlig samtykke ble innhentet fra alle pasienter.
I den innledende behandlingen, karbohydrater ble fordelt over de tre hovedmåltidene. Den første insulin glargine dose ble beregnet til 50% av den forrige total daglig dose, og den første prandial insulin (aspart eller lispro) som de resterende 50% av det totale daglige dose, som ble delt likt å dekke tre måltider., Pasienter som var å ta metformin før du slår den terapi og ikke har noen kontraindikasjon mot det, fortsatte å bruke det på samme dose. Den andre muntlige antidiabetic legemidler ble stoppet.
Alle pasienter deltok på en strukturert ut-pasient-diabetes treningsprogram som består av tre 2-h-gruppen økter i løpet av en uke for 5-8 pasienter. Generelt, de ble lært opp til å følge en diett forutsatt kvalitative karbohydratinntak på hvert måltid, selv for pasienter som ønsket å variere det, karbohydrat-telling måtte gjøres., Pasienter lærte også forvaltningen av basal-bolus terapi og hvordan å justere basal doser insulin i henhold til faste egenkontroll blodsukker (SMBG) hver 7 dager. Justering av prandial insulin dose ble utført i henhold til pre-måltid verdier ved hjelp av en enkel algoritme med faste doser av rask langtidsvirkende insulin. Pasienter som følges opp besøk gitt av sykepleier på 1 og 3 uker, 3 og 6 måneder, og ved endokrinolog ved 2, 4 og 7 måneder, hvor diett ble sjekket og dagbok med SMBG verdier ble gjennomgått for å justere doser insulin., Anthropometric data (vekt, body mass index og livvidde) samt behandling og biokjemiske variabler ble innhentet ved baseline og ved 3 og 6 måneder i alle pasienter. Vi kvantifisert insulinbehovet og antall alvorlig hypoglykemi (definert som krever assistanse) av anamnesis og en gjennomgang av pasientenes dagbøker.
HbA1c var bestemt av høy-ytelse væske-kromatografi (HPLC) (Bio-Rad Laboratories, München, Tyskland), med en referanse rekke 4.6–5.8%., Kolesterol og triglyserider var bestemt av standardiserte enzymatisk metoder og high-density lipoprotein-kolesterol (HDLc) ved en direkte metode (Roche Diagnostics, Basel, Sveits). Low-density lipoprotein-kolesterol (LDLc) ble estimert ved Friedewald formel (hvis triglyserid nivåer var
3.39 mmol/l) eller av ultracentrifugation. Apolipoprotein (Apo) B ble bestemt ved en inmunoturbidimetric metode (Tina-quant, Roche Diagnostics) og LDL størrelse ved elektroforese (2-16%)., Livskvalitet ble målt ved hjelp av en sykdom-spesifikke spørreskjema tilpasset i Spania fra Diabetes livskvalitet (DCCT) ved baseline, og gjentatt på 6 måneder etter basal-bolus insulin terapi.3,4
Data ble analysert ved det statistiske programmet SPSS 15.0 (SPSS Inc.). Endringene i anthropometrical variabler, HbA1c, insulinbehovet og lipid profile ble evaluert av t av Elev-test. De ble betraktet som signifikante verdier av p≤0.05.
Resultater
Den opprinnelige kliniske kjennetegn er oppsummert i Tabell 1., Sytti-åtte prosent av pasientene var under behandling med 2 doser av NPH-eller ferdigblandet insulin forberedelser, 11% av pasientene var å ta muntlig medisiner og sengetid insulin (glargine, detemir eller NPH) og de resterende 11% av pasientene var med andre regimer med 3 doser av NPH og regelmessig insulin. Åtti-sju prosent av pasientene hadde en HbA1c konsentrasjon >8% og 51% hadde HbA1c>9%. Etter å ha byttet til basal-bolus terapi, HbA1c falt fra 9±1.2% til 8,1±1.2% (p
0.001) ved 3 måneder og til 8,0±1.2% ved 6 måneder (p0.001) (Tabell 1, Fig. 1)., Andelen av pasienter med HbA1c≥9% falt fra en innledende 51% (19 saker) til 13.8% og 18.9%, på 3 og 6 måneder henholdsvis. Fig. 2 viser hvor stor andel av pasienter med en HbA1c7%, 7-8% og >8% før og etter bytte til basal-bolus terapi. Fem av pasientene viste en forverring i HbA1c-verdier. Det var bare en episode av alvorlig hypoglykemi er registrert. Ved 6 måneder alle pasientene var i stand til å justere basal insulin dose, men bare 10 pasienter endret prandial dose i henhold til mønstre av SMBG selvstendig.,
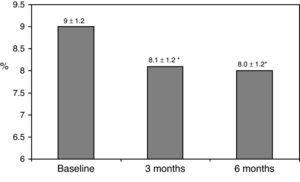
Glycated hemoglobin at baseline and 3 and 6 months after switching to basal-bolus regimen. *p0.001 compared to baseline. HbA1c: glycated hemoglobin.
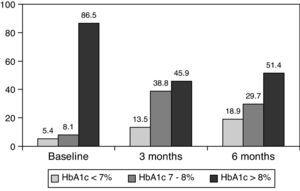
Percentage of patients with glycated hemoglobin 8% at baseline, and 3 and 6 months after switching to basal-bolus regimen.
kroppsvekt, insulinbehovet og lipid parametere ved baseline og under oppfølging er vist i Tabell 1. Kroppsvekt holdt seg stabil i løpet av de 6 månedene av oppfølging og insulinbehovet (UI/kg/dag) ikke endre på 3 måneder, og økte litt ved 6 måneder. Størrelsen på LDL-partikler økt betydelig på 3 (25.77±0.48 nm vs 25.98±0.5 nm, p0.05) og 6 måneder (25.77±0.48 nm vs 25.94±0.44 nm, p0.05), mens den andre lipidiske parametre ble ikke endret.,
Diskusjon
I denne studien, viste vi at basal-bolus insulin terapi kan glykemisk kontroll til å forbedre uten at det går på bekostning av sikkerhet og kvalitet av livet i fag med langsiktig type 2 diabetes, som tidligere er behandlet med en eller flere doser insulin. Vi vil også demonstrere gjennomførbarheten av gjennomføringen av disse insulin regimer gjennom en strukturert ut-pasient treningsprogram.,
Konsensus retningslinjer for behandling av type 2 diabetes mener at det primære mål for behandling er å oppnå HbA1c konsentrasjoner så lavt som mulig uten å forårsake uakseptable hypoglykemi, spesielt hos eldre pasienter eller med koronar sykdom, og for å hindre utvikling av microvascular og macrovascular komplikasjoner.1,5 Dessverre, nyere undersøkelser tyder på at en stor andel av pasienter med diabetes ikke klarer å oppfylle de anbefalte glykemisk mål.,6,7 Selv i National Health and Nutrition Examination Survey (NHANES) andelen av pasienter med HbA1c
7% økt fra 37% i 1999-2000 å 56.8% i 2003-2004, har utbredelsen av suboptimal glykemisk kontroll er spesielt høy hos personer med lignende egenskaper til de som er studert av oss, som har langvarige diabetes eller insulin behandling.,6,7 to Ganger daglig dosering med NPH-eller ferdigblandet insulin som er brukt til å forenkle insulin regimer, men har begrenset fleksibilitet, krever stive tilslutning til vanlige måltider, begrense muligheten til å justere doser av de enkelte komponentene og øke muligheten for hypoglykemi. Dermed, selv om mange pasienter som i utgangspunktet vil oppnå tilstrekkelig glykemisk kontroll med dette regimet,8 når insulin secretory kapasitet på beta-celler er tapt og insulin-mangel er alvorlig, glykemisk kontroll blir dårlig og ustabil som i de fleste av de pasientene som ble inkludert i denne studien.,1,8 Vi viste at hos pasienter med langvarige, type 2 diabetes, dårlig kontrollert med andre regimer av insulin og ustabil profil, basal-bolus insulin diett reduserer HbA1c ett poeng over 6 måneder, og andelen av pasienter med HbA1c≥9% fra 51% til 14% ved 3 måneder og 19% på 6 måneder. Dette er sannsynligvis fordi det er en mer fysiologisk behandling, mens prandial insulin erstatter første fase endogene insulin sekresjon, basal insulin senker nivået av fastende hyperglykemi., Dermed, i tillegg til nivået av HbA1c 9 slik behandling er intensivert i stor grad endrer den relative bidrag av basal og postprandial hyperglykemi til den generelle hyperglykemi av T2DM pasienter. Nylig, Gåte et al.10 viste at etter behandling intensivering med insulin, bidrag fra basal hyperglykemi dråper, men fortsatt står for om lag en tredjedel av det som er att hyperglykemi. Derfor, i henhold til funnene i denne undersøkelsen, bruk av insulin regimer som kombinerer basal med prandial insulin vil ofte være nødvendig for å oppnå glykemisk mål., Faktisk, disse funnene er i samsvar med de aller bevis for fordelene av basal-bolus terapi i type 1 diabetes 11 og støttes av den begrensede data fra observasjonelle studier hos pasienter med type 2 diabetes bytte fra premix til basal-bolus glargine-basert diett 12,13 og ved en randomisert sammenligning av en premix-basert diett mot et basal-bolus regime i type 2 diabetiker pasienter.2,14,15 hos pasienter tidligere behandlet med glargine pluss muntlig anti-diabetiker medisiner, forskjellen i HbA1c var 0.,22% i favør av basal-bolus glargine-basert diett, i forhold til en ferdigblandet insulin regimen15. I de FORETREKKER å studere,14 undergruppen av pasienter tidligere på en basal insulin diett viste en større reduksjon av HbA1c med detemir/aspart basal-bolus diett sammenlignet med bifasisk insulin aspart (-1.21% vs -0.75%). Til slutt, i premix behandlet type 2 diabetiker pasienter, Fritsche et al. viste at et basal-bolus glargine/glulisine-basert insulin regime var overlegen til en premix insulin regime i reduksjon av HbA1c (-1.31% vs 0.8%).,2 Derfor, selv om det er forskjeller i omfanget av forbedring mellom studier, sannsynligvis på grunn av de forskjellige baseline karakteristikker av den studerte populasjonen, overlegenhet av et basal-bolus regime i utvalgte pasienter med langvarige sykdom synes demonstrert. Reduksjon av mer enn ett poeng av HbA1c oppnås ved å bytte til et basal-bolus insulin diett kan anses å være klinisk signifikante fordi det kan resultere i reduksjon av kliniske resultater., Dessverre, basal-bolus terapi er underutnyttet i pasienter med T2DM fordi leger anser det for komplisert å gjennomføre, det er tidkrevende og det er frykt for økt antall injeksjoner, er risikoen for hypoglykemi, vektøkning og forverring av livskvalitet. I denne og tidligere studier kroppsvekt og frekvensen av alvorlig hypoglykemi ble ikke økt,2,12, som kan være knyttet til mer fysiologisk insulin substitusjon med basal-bolus diett og fleksibiliteten som denne behandling kan tilbys til pasienter., Derfor, frykt for hypoglykemi bør ikke være en barriere for å starte denne typen behandling i T2DM, men det har også å bli vurdert for å etablere glykemisk kontroll mål som det kan føre til sykelighet og økt dødelighet.16 Om effekten på livskvalitet, i samstemmighet med rapporten av Ménard et al.17 om vår studie ikke støtter det syn at basal-bolus regimer føre til en redusert livskvalitet.
Ifølge en tidligere rapport,12 i undersøkelsen alle pasienter som var i stand til å kunne titrere sine basale insulin dose i henhold til faste SMBG av de siste 3-7 dager., I kontrast, er det få pasienter som var i stand til å justere prandial doser insulin i henhold til mønstre av SMBG og mest behov for støtte fra en enkel algoritme med faste dose avhengig premeal blodsukker. Dette er ikke overraskende siden å etablere den optimale måltid insulin dose ofte innebærer beregninger som tar hensyn til flere faktorer og er vanskelig for noen pasienter. Videre, ved hjelp av en enkel algoritme for å justere måltid rask langtidsvirkende insulin hver uke basert på SMBG mønstre er like effektivt som å justere måltid insulin ved hjelp av insulin-til-karbohydrat prosenter i T2DM fag.,18
Begrensninger med studien er knyttet til den prospektive observasjonelle design og mangel på kontroll gruppe. Disse aspektene, og den korte oppfølging av pasienter, og vanskelig å tolke funnene og deres anvendelse på pasienter med T2DM som følges i andre sentre. Imidlertid, selv om fremtidige studier i større grupper av pasienter som bør utføres for å bekrefte disse funnene, studien gir informasjon som kan være nyttig for behandling av en felles og dårlig behandlet kliniske situasjonen.,
I en konklusjon denne studien har vist at en 9-timers ut-pasient program tillatt lang varighet T2DM pasienter dårlig kontrollert med andre insulin regimer for å bytte til basal-bolus insulin diett. Vi har også bekreftet at basal-bolus insulin-behandlingen er effektiv, trygg og ikke forringe kvaliteten på livet i denne undergruppen av T2DM pasienter. Dermed basal-bolus terapi kan bli tilbudt å T2DM fag som ikke er kontrollert med andre insulin strategier.
interessekonflikt
Irene Vinagre har mottatt foredrag avgifter fra Eli Lilly, Novo Nordisk og Sanofi Aventis., Antonio Perez har mottatt con sulting og foredrag avgifter fra Eli Lilly, Novo Nordisk og Sanofi Aventis.