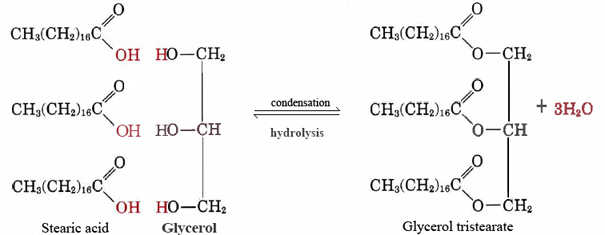
Un buon esempio di un lipido non polare è il tristearato di glicerolo grasso neutro. Questa forma più comune di grasso animale funge da magazzino per l’energia e come isolamento contro la perdita di calore. A livello molecolare è costruito da tre molecole di acido stearico e una di glicerolo:
 (1)
(1)
Un gran numero di lipidi non polari può essere fatto combinando diversi acidi a catena lunga con glicerolo., Poiché questi acidi erano originariamente derivati dai grassi, sono collettivamente indicati come acidi grassi.
Si noti che per ogni molecola di acido grasso stearico o altra che si combina con uno dei gruppi —OH di glicerolo, viene emessa una molecola di acqua e quindi la reazione è una condensazione. Si scopre che molte importanti molecole biologiche sono messe insieme da reazioni di condensazione durante le quali l’acqua viene emessa. Il contrario di Eq. (1), in cui l’acqua reagisce con una grande molecola e la divide in pezzi più piccoli, è chiamata idrolisi., Effettuando l’idrolisi gli organismi viventi possono abbattere le molecole prodotte da altre specie. I semplici blocchi di costruzione ottenuti in questo modo possono quindi essere ricombinati da reazioni di condensazione per formare strutture appropriate al loro nuovo ospite.
A differenza del tristearato di glicerolo presente negli animali, i grassi vegetali contengono numerosi doppi legami nelle loro lunghe catene idrocarburiche. Questa polinsaturazione introduce “nodi” nelle catene idrocarburiche a causa della barriera alla rotazione e degli angoli di 120° associati ai doppi legami., Di conseguenza è più difficile allineare le catene fianco a fianco (vedi Figura \(\PageIndex{1}\)) e i grassi insaturi non si raggruppano facilmente in un reticolo cristallino. Come era vero con alcani, lunghezza della catena determina anche se un grasso è liquido o solido, e dove si verifica il punto di fusione.
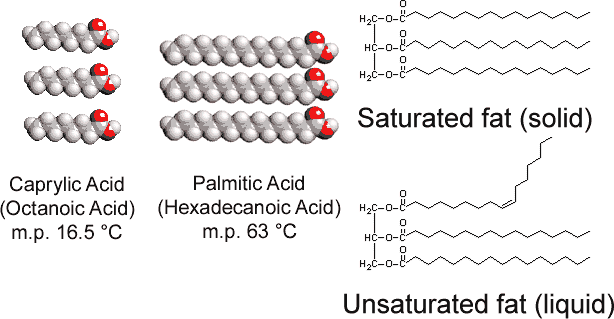
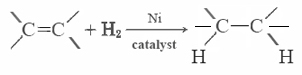
La maggior parte dei grassi insaturi (come l’olio di mais) sono liquidi a temperature normali, mentre i grassi saturi (come il burro) sono solidi. Gli oli vegetali possono essere convertiti per idrogenazione in composti solidi. Questo processo comporta l’aggiunta di H2 cataliticamente ai doppi legami:
L’idrolisi dei grassi è importante nella produzione di saponi., Può essere accelerato dall’aggiunta di una base forte come NaOH o KOH, nel qual caso la reazione è chiamata saponificazione. Poiché la saponificazione richiede che il pH della miscela di reazione sia alto, l’acido grasso che viene prodotto si dissocia al suo anione. Quando il glicerolo tristearato viene saponificato con NaOH, ad esempio, si forma lo stearato di sodio, una sostanza relativamente solubile in acqua e un sapone comune.
La capacità dei saponi di pulire grasso e olio dalle superfici sporche è il risultato delle doppie strutture idrofobo-idrofile delle loro molecole., Lo ste stearato, ad esempio, è costituito da una lunga catena idrocarburica non polare con un gruppo COO altamente polare ad un’estremità.
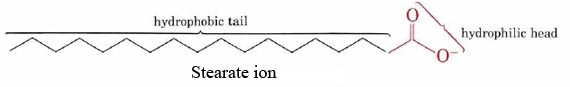
La catena idrocarburica idrofobica cerca di evitare il contatto con mezzi acquosi, mentre il gruppo anionico accoglie prontamente le attrazioni di dipolo e i legami idrogeno delle molecole d’acqua.
I due modi principali in cui le porzioni idrofobiche di ioni stearato possono evitare l’acqua sono di raggrupparsi sulla superficie o di dissolversi in una piccola quantità di olio o grasso (vedi Figura \(\PageIndex{2}\) ).,
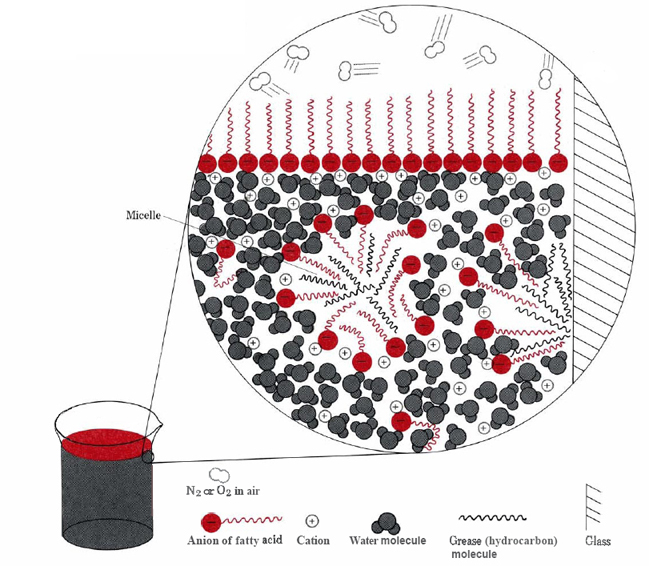
In quest’ultimo caso le teste idrofile delle molecole di sapone entrano in contatto con l’acqua all’esterno del grasso, formando una struttura nota come micella. Poiché gli esterni delle micelle sono caricati negativamente, si respingono l’un l’altro e impediscono alle goccioline di grasso di ricombinarsi., Il grasso viene quindi sospeso (emulsionato) nell’acqua e può essere lavato via facilmente.
I saponi naturali, come lo stearato di sodio, erano originariamente prodotti in casa riscaldando il grasso animale con ceneri di legno, che contenevano potassio, K2CO3. Grandi quantità sono ancora prodotte industrialmente, ma in misura considerevole i saponi sono stati sostituiti da detergenti. Questa è una conseguenza del comportamento indesiderato dei saponi in acqua dura. Calcio, magnesio e altri cationi di acqua dura formano composti insolubili quando combinati con gli anioni degli acidi grassi., Questo produce precipitati scummy e impedisce le molecole di sapone da emulsionare grasso a meno che non viene utilizzato un grande eccesso.
Detergenti come alchilbenzensolfonati (ABS) e alchilbenzensolfonati lineari (LAS) hanno strutture molto simili a stearato di sodio, tranne che il gruppo caricato nelle loro teste idrofile è —SO3– attaccato ad un anello benzenico. I detergenti ABS hanno anche gruppi metilici (CH3) che si ramificano dalle loro catene di idrocarburi.,
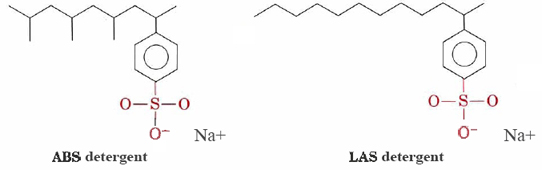
Tali molecole non precipitano con cationi di acqua dura e quindi sono più adatte per il lavaggio in lavatrice di vestiti. I detergenti LAS sostituirono l’ABS durante la metà degli anni Sessanta, quando si scoprì che questi ultimi non erano biodegradabili. Stavano facendo sì che i fiumi e persino l’acqua del rubinetto si ricoprissero di schiuma detergente e schiuma. Apparentemente gli enzimi nei microrganismi che si erano evoluti per abbattere le catene idrocarburiche non ramificate nei grassi naturali e negli acidi grassi erano incapaci di digerire le catene ramificate delle molecole di ABS., I detergenti LAS, sebbene fabbricati dall’uomo, imitano le strutture delle molecole presenti in natura e sono biodegradabili.