Exception 2: Octets incomplets
la deuxième exception à la règle D’Octet est quand il y a trop peu d’électrons de valence qui entraîne un Octet incomplet. Il y a encore plus d’occasions où la règle de l’octet ne donne pas la représentation la plus correcte d’une molécule ou d’un ion. C’est également le cas des octets incomplets. Les espèces avec des octets incomplets sont assez rares et ne se trouvent généralement que dans certains composés du béryllium, de l’aluminium et du bore, y compris les hydrures de bore., Jetons un coup d’œil à un tel hydrure, \(BH_3\) (Borane).
Si l’on devait faire une structure de Lewis pour \(BH_3\) en suivant les stratégies de base pour dessiner des structures de Lewis, on trouverait probablement cette structure (Figure 3):
le problème avec cette structure est que le bore a un octet incomplet; il n’a que six électrons autour de lui., Les atomes d’hydrogène ne peuvent naturellement avoir que 2 électrons dans leur enveloppe la plus externe (leur version d’un octet), et en tant que tel, il n’y a pas d’électrons de rechange pour former une double liaison avec le bore. On pourrait supposer que l’échec de cette structure à former des octets complets doit signifier que cette liaison devrait être ionique au lieu de covalente., Cependant, le bore a une électronégativité qui est très similaire à l’hydrogène, ce qui signifie qu’il y a probablement très peu de caractère ionique dans les liaisons hydrogène-bore, et en tant que telle cette structure de Lewis, bien qu’elle ne remplisse pas la règle de l’octet, est probablement la meilleure structure possible pour représenter BH3 avec la L’une des choses qui peuvent expliquer L’octet incomplet de BH3 est qu’il s’agit généralement d’une espèce transitoire, formée temporairement dans des réactions impliquant plusieurs étapes.
examinons une autre situation d’octet incomplet traitant du bore, BF3 (trifluorine de bore)., Comme avec BH3, le dessin initial d’une structure de Lewis de BF3 formera une structure où le bore n’a que six électrons autour de lui (Figure 4).
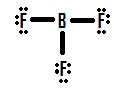
Si vous regardez la Figure 4, Vous pouvez voir que les atomes de fluor possèdent des paires solitaires supplémentaires qu’ils peuvent utiliser pour créer des liaisons supplémentaires avec le bore, et faire est de faire une paire solitaire dans une liaison et la structure sera correcte., Si nous ajoutons une double liaison entre le bore et l’un des fluor, nous obtenons la Structure de Lewis suivante (Figure 5):
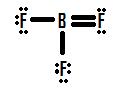
chaque fluor a huit électrons, et la l’atome de bore en a huit aussi! Chaque atome a un octet parfait, non? Pas si vite. Nous devons examiner les charges formelles de cette structure. Le fluor qui partage une double liaison avec le bore a six électrons autour de lui (quatre de ses deux paires d’électrons solitaires et un chacun de ses deux liaisons avec le bore)., C’est un électron de moins que le nombre d’électrons de valence qu’il aurait naturellement (les éléments du groupe sept ont sept électrons de valence), donc il a une charge formelle de +1. Les deux flourines qui partagent des liaisons simples avec le bore ont sept électrons autour d’eux (six de leurs trois paires solitaires et un de leurs liaisons simples avec le bore). C’est la même quantité que le nombre d’électrons de valence qu’ils auraient eux-mêmes, donc ils ont tous deux une charge formelle de zéro. Enfin, le bore a quatre électrons autour de lui (un de chacune de ses quatre liaisons partagées avec le fluor)., C’est un électron de plus que le nombre d’électrons de valence que le bore aurait seul, et en tant que tel, le bore a une charge formelle de -1.
Cette structure est étayée par le fait que la longueur de liaison déterminée expérimentalement des liaisons bore-fluor dans BF3 est inférieure à ce qui serait typique pour une seule liaison (voir ordre et longueurs de liaison)., Cependant, cette structure contredit l’une des règles majeures des charges formelles: les charges formelles négatives sont supposées se trouver sur le ou les atomes les plus électronégatifs d’une liaison, mais dans la structure représentée à la Figure 5, une charge formelle positive se trouve sur le fluor, qui est non seulement l’élément le plus électronégatif de la structure, mais l’élément le plus électronégatif de tout le tableau périodique (\(\chi=4.0\)). Le bore d’autre part, avec l’électronégativité beaucoup plus faible de 2,0, A la charge formelle négative dans cette structure., Ce désaccord formel charge-électronégativité rend cette structure à double liaison impossible.
cependant, la grande différence d’électronégativité ici, par opposition à BH3, signifie des liaisons polaires importantes entre le bore et le fluor, ce qui signifie qu’il y a un caractère ionique élevé à cette molécule. Cela suggère la possibilité d’une structure semi-ionique telle que vue sur la Figure 6:

aucune de ces trois structures n’est la structure « correcte » dans ce cas., La structure la plus » correcte » est très probablement une résonance des Trois structures: celle avec l’octet incomplet (Figure 4), celle avec la double liaison (Figure 5) et celle avec la liaison ionique (Figure 6). La structure la plus contributive est probablement la structure d’octet incomplète (en raison de la Figure 5 étant fondamentalement impossible et de la Figure 6 ne correspondant pas au comportement et aux propriétés de BF3). Comme vous pouvez le voir même lorsque d’autres possibilités existent, les octets incomplets peuvent mieux représenter une structure moléculaire.,
en guise de remarque, il est important de noter que BF3 se lie fréquemment avec un ion F afin de former BF4 – plutôt que de rester BF3. Cette structure complète l’octet de bore et il est plus commun dans la nature. Ceci illustre le fait que les octets incomplets sont rares, et d’autres configurations sont généralement plus favorables, y compris la liaison avec des ions supplémentaires comme dans le cas de BF3 .
exemple: \(BF_3\)
dessinez la structure de Lewis pour le trifluorure de bore (BF3).
la Solution
1. Ajouter des électrons (3*7) + 3 = 24
2., Dessiner des connectivités:
3. Ajouter des octets à l’extérieur des atomes:
4. Ajouter des électrons (24-24=0) à l’atome central:
5. Le centre d’électrons ont octet?
- PAS de. Il a 6 électrons
- Ajouter une liaison multiple (double liaison) pour voir si l’atome central de parvenir à un octet:
6. Le bore central a maintenant un octet (il y aurait trois structures de Lewis de résonance)
cependant…,
- Dans cette structure à double liaison, l’atome de fluor partage des électrons supplémentaires avec le bore.
- Le fluor aurait une charge partielle »+ », et le bore une charge partielle » -« , ce qui est incompatible avec les électronégativités du fluor et du bore.
- ainsi, la structure de BF3, avec des liaisons simples, et 6 électrons de valence autour du bore central est la structure la plus probable
- BF3 réagit fortement avec des composés qui ont une paire d’électrons non partagée qui peut être utilisée pour former une liaison avec le bore: