A Microbial Biorealm page on the genus Enterobacter aerogenes
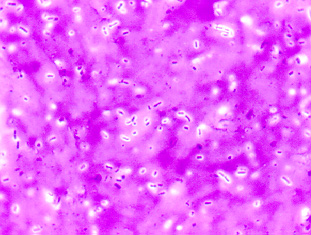
Classification
taxons D’ordre supérieur
bactéries; Proteobacteria; Gammaproteobacteria; Enterobacteriales; Enterobacteriaceae; Enterobacter
espèces
Enterobacter aerogenes
des Discussions sur la véritable taxonomie de E. aerogenes existent actuellement en raison de la distance génomique entre E. cloaque et Klebsiella. La recherche montre que E. aerogenes est plus étroitement lié à Klebsiella (47-64%) que E. cloacae (44%).,
Description et signification
La famille des Enterobacteriaceae comprend les genres Escherichia, Shilgella, Salmonella, Enterobacter, Klebsiella, Serratia, Proteus, entre autres. La bactérie à gram négatif réside dans le sol, l’eau, les produits laitiers et habite une flore naturelle dans le tractus gastro-intestinal des animaux ainsi que des humains., Les entérobactéries en forme de bâtonnet existent dans une variété de tailles; ne forment pas de spores; sont à la fois mobiles (avec des flagelles péritriches) ou non molles; poussent à la fois aérobiquement et anaérobiquement; sont actifs biochimiquement; fermentent (versus oxydent) le D-glucose ainsi que d’autres sucres, souvent avec production de gaz; réduisent le nitrate en nitrite; contiennent l’antigène commun enterobacter; et ont une teneur en ADN de 39 à 59% en guanine plus cytosine (G + C) (2).,
Le genre Enterobacter est plus spécifiquement un pathogène opportuniste nosocomial et est recherché pour être l’une des nombreuses causes clés des infections extra-intestinales à côté d’E. coli. Les Infections communément attribuées à E. aerogenes sont les infections respiratoires, gastro-intestinales et urinaires, en particulier les cystites, en plus des infections des plaies, de la circulation sanguine et du système nerveux central (1,2,3). De plus, E. cloacea et E. aerogenes sont les espèces les plus couramment associées aux cas de méningite. Les Colonies de souches D’Enterobacter peuvent être légèrement mucoïdes.,
en milieu clinique, Enterobacter aerogenes et Enterobacter cloacae sont les plus fréquemment isolés dans des échantillons de patients hospitalisés infectés. La majorité des infections sont étiologiquement dues au transfert involontaire de bactéries pendant la chirurgie ou le traitement prolongé dans les hôpitaux chez les patients qui utilisent des cathéters veineux ou urétraux. Les entérobactéries peuvent représenter 80% des isolats cliniquement significatifs de bacilles à gram négatif et 50% des bactéries cliniquement significatives dans les laboratoires de microbiologie clinique., En outre, ils représentent près de 50% des cas de septicémie et plus de 70% des infections des voies urinaires et intestinales. La gravité de ces infections crée donc une importance pour cibler, isoler, identifier et tester la sensibilité aux causes de ces infections nosocomiales (2).
structure du génome
E. Les aerogenes sont des cellules plus petites, en forme de bâtonnet, qui sont mobiles et encapsulées par rapport aux autres cellules de la même famille D’entérobactéries., L’information génomique complète (88% est codée) n’a pas encore été entièrement séquencée, cependant, certaines recherches montrent des études sur les mutations et montrent des preuves de réplication par le biais de plasmides. Les échantillons de taches d’E. cloacae et d’E. aerogenes ne présentaient aucun élément extrachromosomique (9). L’analyse des plasmides reste l’une des techniques de laboratoire les plus utilisées, mais le PFGE, le RAPD, le ribotypage, le consensus intergénique répétitif entérobactérien (ERIC), la PCR et le polymorphisme de longueur de fragment amplifié sont également utilisés. Le nom du réplicon est R751. La bactérie est constituée d’ADN et est circulaire., Sa longueur est de 53 435 paires de base et ne contient aucun ARN structurel. La teneur en G + C est de 64% et aucun gène psuedo n’est enregistré pour E. aerogenes (9).
structure cellulaire et métabolisme
Enterbacter aerogenes est une bactérie gram-négative en forme de bâtonnet qui contient des flagelles entourant sa surface externe. E. aerogenes ainsi que d’autres de son genre sont connus pour être résistants aux antibiotiques, en particulier E. aerogenes et E. cloacae. La recherche montre que deux souches cliniques de E., aerogenes a présenté des phénotypes de multirésistance aux antibiotiques β-lactamines, aux fluoroquinolones, au chloramphénicol, à la tétracycline et à la kanamycine. Les deux souches ont montré un profil de porine différent de celui d’une souche sensible. Ils ont eu une réduction drastique de la quantité de porine majeure mais avec une structure normale apparemment conservée (taille et immunogénicité), ainsi qu’une surproduction de deux protéines membranaires externes connues, OmpX et LamB (8).
Écologie
Enterobacter se trouvent dans le sol, l’eau, les produits laitiers, et dans les intestins des animaux ainsi que les humains., Ils se trouvent le plus souvent dans le tractus gastro-intestinal et sont étudiés dans des sites cliniques dans des échantillons de selles. Le pH minimum, optimal et maximal pour la réplication D’E. aerogenes est de 4,4, 6,0-7,0 et 9,0 (6).
Enterobacter aerogenes a été plaqué sur plusieurs supports différents et a été observé dans le cadre de plusieurs types de tests. Les résultats sont les suivants – E. aerogenes testé négatif lorsqu’il est traité avec/pour: Indol, rouge de méthyle, sulfure d’hydrogène (par voie de TSI), uréase, Arginine dihydrolase, Phénylalanine désaminase et Dulcitol. E., aerogenes a été testé positif lorsqu’il a été traité avec / pour: Voges-Proskauer, citrate de Simmons, KCN, motilité, Lysine décarboxylase, Ornithine décarboxylase, gaz de glucose, Lactose, saccharose, Manntiol, salicine, Adonitol, Inositol, Sorbitol, Arabinose, Raffinose et Rhamnose. Des résultats positifs différés ont été obtenus à partir de: gélatine (22°C) et Malonate (11). En d’autres termes, E. aerogenes ressemble à E. cloacae mais le test de la décarboxylase de la leusine est positif et la liquéfaction de la gélatine est tardive. E. aerogenes est aussi, souvent confondu avec Klebsiella aerogenes. Cependant, E., aerogenes est motile et uréase négative tandis que K. aerogenes est non motile et uréase positive (5). En réalité ,la recherche montre que » E. aerogenes est plus lié à Klebsiella aerogenes (47-64%) qu’à E. cloacae (44%) (9).
différentes espèces D’entérobactéries comme E. cloacae sont connues pour être trouvées sur un certain nombre de graines et de plantes, tandis que E. sakazakii est couramment observée chez les nourrissons qui ont reçu des préparations en poudre à base de lait infantile (9).
pathologie
Enterobacter aerogenes provoque des maladies chez l’homme par transfert involontaire de bactéries en milieu hospitalier., Une sélection de bactéries entériques comme E. aerogenes sont opportunistes et n’infectent que ceux qui ont déjà supprimé les défenses immunitaires de l’hôte. Les nourrissons, les personnes âgées et ceux qui sont en phase terminale d’une autre maladie ou qui sont immunodéprimés sont les principaux candidats à de telles infections (9).
En outre, E. aerogenes ainsi que d’autres bactéries entériques, est connu pour avoir des caractéristiques de résistance aux médicaments. Il y a eu un certain succès dans le traitement des infections par antibiotiques, cependant, le développement rapide de la multirésistance aux médicaments est devenu un problème de plus en plus croissant (3)., Ces souches multirésistantes ont provoqué des éclosions dans des unités de soins intensifs (USI) en Belgique, en France, en Autriche et aux États-Unis et sont devenues plus émergentes que son espèce sœur E. cloacaw (12). La recherche a montré que E. aerogenes est résistant à l’ampicilline et il a été découvert récemment qu’il est résistant à l’imipenem (11).
en général, les mécanismes pathogènes exprimés par les souches D’Enterobacter sont inconnus. Comme d’autres souches telles que Klebsiella, elles expriment la fimbraie de type 1 et de type 3., La plupart des souches expriment également des systèmes d’absorption de fer médiés par l’aérobactine, généralement associés à des agents pathogènes bactériens humains extra-intestinaux. Certaines souches peuvent produire une hémolysine ressemblant à l’α-hémolysine produite par les souches d’E. coli. De plus, une protéine de la membrane externe, OmpX, peut être un facteur pathogène pour les souches E. cloacae. Cette protéine particulière semble réduire la production de porines sur les bactéries à gram négatif, entraînant une diminution de la sensibilité aux antibiotiques β-lactamines et pourrait donc jouer un rôle dans l’invasion cellulaire de l’hôte (7).,
Les espèces D’entérobactéries produisent des hémagglutinines sensibles au mannose de type 1 ou 3 (MSHA) et produisent rarement des hémagglutinines résistantes au mannose. La seule exception étant E. gergoviae. En outre, la production d’une variété de sidérophores par les entérobactéries est également couramment observée. E. cloacae génèrent l’aérobactine sidérophore hydroxyamate, qui est couramment utilisée avec les espèces microbiennes qui causent la maladie d’invasion. De plus, plusieurs toxines ont été produites par des espèces D’entérobactéries., Habituellement, ces toxines sont décrites comme ayant des souches uniques ou sont limitées dans le nombre d’isolats (9).
des mesures préventives peuvent être prises pour réduire L’infection D’E. aerogenes en surveillant attentivement les techniques chirurgicales aseptiques (3). Les cathéters doivent être retirés et les aiguilles veineuses et les tubes doivent être retirés et placés dans de nouveaux endroits. Le traitement d’E. aerogenes est difficile en raison de la nature très résistante de l’espèce. Les souches d’Enterobacter sont résistantes aux pénicillines et autres céphalosporines en raison de la production de bêta-lactamase chromosomique avec une activité cépholosprinase., En outre, beaucoup sont résistants à la tétracycline, au chloramphénicol et à la streptomycine, ainsi qu’à d’autres aminoglycosides (tels que la gentamicine et les fluoroquinolones). La plupart des souches peuvent sembler sensibles à la céfotaxime lors des tests primaires, mais elles possèdent souvent une céphalosporinase chromosomique inductible, ce qui permet le développement rapide d’une résistance pendant le traitement ou le traitement (7).
facteurs de risque pour les entérobactéries nosocomiales comme E., les infections à aerogenes comprennent une hospitalisation de plus de 2 semaines, des procédures invasives au cours des 72 dernières heures, un traitement antibiotique au cours des 30 derniers jours et la présence d’un cathéter veineux central. Les facteurs de risque spécifiques d’infection par des souches nosocomiales multirésistantes d’espèces D’entérobactéries doivent être pris en compte et comprennent l’utilisation récente de céphalosporines à large spectre ou d’aminoglycosides et les soins intensifs (13).,
en plus du spectre élargi des céphalosporines, Enterobacter aerogenes a récemment montré une résistance aux carbapénèmes chez un mâle chinois de 39 ans à la suite d’une greffe de foie cadavérique. On pensait que l’infection initiale était liée aux caractéristiques immunosuppressives de la chimiothérapie que l’homme recevait pour un cancer du foie, facilitant le déplacement des micro-organismes du tractus intestinal vers le sang et d’autres parties du corps. Après l’opération mais avant le traitement au carbapénème, une souche sensible au carbapénème de E., aerogenes a été extrait de la bile, de la Dopsie abdominale et du sang. Malgré le traitement au carbapénème, le patient a développé plusieurs abcès dans la région abdominale, conduisant finalement à une deuxième greffe du foie deux mois plus tard, au cours de laquelle E. aerogenes résistant au carbapénème a été isolé du sang et du liquide abdominal. Le patient a ensuite développé un choc septique et un syndrome de dysfonctionnement de plusieurs organes résultant de la réponse immunitaire et systémique aux bactéries résistantes. (18).,
La résistance au carbapénème peut apparaître après 40 jours de résistance au carbapénème et son mécanisme peut être directement corrélé à la perte du gène OmpE36 ainsi qu’à la production de plusieurs bêta-lactamases qui confèrent également sa résistance à d’autres antibiotiques à large spectre. Dans l’ensemble, ces résultats sont regrettables car les carbapénèmes sont « presque un dernier recours en infection terminale. »Pour de tels scénarios, des propositions d’utilisation de” vieux » médicaments tels que la colistine ont été faites, malgré leur grande néphro-et neurotoxicité (18.,)
Enterobacteriaceae aerogenes provoquent une variété d’infections, souvent transmises en milieu hospitalier. Plus important encore, Enterobacteriaceae aerogenes a montré une résistance multidrogue due en grande partie à des mutations qui codent les porines (canaux protéiques) et des pompes d’efflux membranaires qui pompent les antibiotiques avant qu’ils ne puissent nuire à l’organisme. Ceux-ci se sont avérés non spécifiques, ce qui explique leur résistance aux médicaments multiples. Des molécules structurellement non apparentées telles que les antibiotiques B-lactamines, les quinolones, les tétracyclines et le chloramphénicol sont toutes maintenues à distance., Les nouveaux médicaments ciblant cette bactérie doivent se concentrer sur cette ligne de défense bactérienne, et cette étude spécifique a porté sur plusieurs dérivés d’alkoxyquinoléine ou composés de quinoléine 4-alkoxysubstitués. L’un de ces composés particuliers, marqué « composé 905”, a été montré pour induire l’inhibition de la pompe de chloramphénicol, permettant au chloramphénicol d’entrer dans la membrane bactérienne, augmentant les concentrations de celui-ci à l’intérieur de la cellule. La perméabilité membranaire a été testée pour s’assurer que les résultats n’étaient pas influencés par les effets secondaires des composés augmentant la perméabilité membranaire., Il a été démontré que le composé n’augmentait pas significativement la perméabilité de la membrane, ce qui indique un effet unique et spécifique sur l’activité de la pompe au chloramphénicol. Quatre des souches cliniques testées présentaient une sensibilité accrue à la norfloxacine, à la tétracycline et au chloramphénicol, qui étaient auparavant maintenus à l’extérieur de la cellule par des pompes d’efflux. Le composé 905 a inhibé ces pompes, permettant aux antibiotiques d’accumuler des concentrations significatives à l’intérieur des cellules (23).
Application à la biotechnologie
des études montrent que E. aerogenes a un taux de résistance aux médicaments croissant., Des niveaux élevés de résistance aux médicaments chez les entérobactéries ont été trouvés conformément aux aminoglycosides et à la ceftazidime à large spectre et de quatrième génération (>40%) et à la céfépime (15%). Les taches d’E. aerogenes ont montré la production de β-lactamases à spectre étendu (ESBL). Une résistance telle que celle-ci survient souvent de novo chez les patients recevant un traitement empirique pour les infections systémiques. Ces entérobactéries résistantes aux médicaments peuvent apparaître plus tard pour produire des maladies graves ou fulminantes chez les patients immunodéprimés (9). La résistance aux médicaments tels que ceux-ci sont des produits courants D’Enterobacter., Plusieurs traitements médicamenteux semblent être efficaces, cependant, après un traitement prolongé, une résistance apparaît et de nouveaux médicaments doivent être administrés.
Les mécanismes de résistance impliqués par les souches d’E. aerogenes sont associés à des altérations de la membrane externe qui provoquent une diminution de la porine et des modifications des lipopolysaccharides. En raison de sa résistance aux antibiotiques, de nombreux chercheurs sont revenus aux « anciens médicaments » tels que la colistine en plus de l’imipénème pour traiter les infections graves à E. aerogenes.,
recherche actuelle
dans une étude de cas utilisée pour déterminer la cause des infections de l’aorte, l’isolement de deux souches: S. pneumoniae et E. aerogenes a été découvert et extrait d’un mâle de 72 ans souffrant de douleurs épigastriques, de fièvres et de frissons. L’origine de E. aerogenes est inconnue, mais on pense qu’elle est le résultat d’une infection des voies urinaires ou d’une pneumonie non diagnostiquée. Les recherches antérieures indiquent que cette étude de cas n’est que le deuxième rapport dans la littérature mentionnant plusieurs organismes dans L’aortite infectieuse concernant E. aerogenes et S. pneumoniae., En plus de cela, Enterobacter n’a été signalé que comme une cause d’aortite infectieuse dans le cadre de greffes aortiques. C’est la première fois Qu’Enterobacter est signalé dans l’aortite infectieuse cryptogénique. L’étude a conclu que les infections de l’aorte sont rares, sont causées par divers agents pathogènes, et sont difficiles à diagnostiquer. Les symptômes que les patients peuvent ressentir comprennent de la fièvre et des douleurs abdominales (et une masse abdominale palpable et pulsatile si l’aorte est anévrismale). Les hémocultures, si elles sont positives, peuvent être utiles, tout comme le CTA et l’imagerie scintigraphique leucocytaire., Un indice élevé de suspicion est nécessaire car la mortalité, si seulement traitée médicalement, approche 100%. Le traitement chirurgical et médical combiné est supérieur, réduisant le taux de mortalité entre 20% et 60% (14).
le locus Eefabc D’Enterobacter aerogenes, qui code une pompe d’efflux tripartite, a été cloné par complémentation d’un mutant TOLC D’Escherichia coli. E. aerogenes est devenu moins sensible à une large gamme d’antibiotiques., Les données de fusions eef:: lacZ ont montré que l’eefABC n’était pas transcrite dans les diverses conditions de laboratoire testées, mais augmentait la transcription à partir de Peef (à partir d’un mutant hns D’E. coli). De plus, L’EefA a été détectée chez E. aerogenes exprimant un allèle HNS d’E. coli négatif dominant. La recherche a conclu que de nombreux gènes cibles H-NS sont impliqués dans l’adaptation bactérienne aux conditions environnementales stressantes et à la virulence. La pertinence biologique du silençage de l’opéron eef n’est toujours pas connue. Cependant, comme d’autres bactéries commensales ou pathogènes, E., aerogenes doit subir des changements drastiques dans son profil d’expression génique afin de s’adapter aux conditions associées à l’hôte (15).
D’autres entérobactéries sont observées, en particulier celles concernant L’espèce Enterobacter sakazakii qui est un agent pathogène transmis par les préparations pour nourrissons qui provoque une méningite sévère, une méningo-encéphalite, une septicémie et une entérocolite nécrosante chez les nouveau-nés et les nourrissons, créant un taux de mortalité élevé. Le gène de la protéine a de la membrane externe (ompA) et des séquences d’E. sakazakii (ATCC 51329) ont été clonés dans le vecteur pGEM-T Easy et séquencés., Un haut degré d’homologie avec les gènes ompA d’autres bactéries gram-négatives appartenant aux Enterobacteriaceae a été découvert lorsque les séquences de nucléotides et d’acides aminés déduits ont été comparées à celles de GenBank. Les protéines ont une identité de 89% et une conservation de séquence de 94% au niveau des acides aminés. De même, le gène ompA d’E. sakazakii avait des identités de séquence de 86% et 88% aux niveaux des acides nucléiques et des acides aminés. En outre, avec Enterobacter aerogenes, 87% et 90% avec serovar Typhimurium, et 85% et 88% avec Shigella flexneri., Une analyse de prédiction du site de clivage des peptides de signaux a ainsi révélé une séquence de signaux N-terminaux à 21 acides aminés similaire à celles trouvées chez E. coli, E. aerogenes, S. flexneri et S. enterica serovar Typhi (16).
des recherches récentes ont été menées dans l’espoir d’identifier une corrélation entre la présence de plasmides codés par la bêta-lactamase à spectre étendu (« ESBL”) et la résistance aux médicaments de différentes bactéries à gram négatif. En utilisant six espèces différentes, y compris” Enterobacter aerogenes », des données ont été collectées pour essayer de mesurer l’effet de la BLSE., Sur les six espèces étudiées, toutes, sauf une, étaient positives pour le plasmide ESBL. À leur tour, ils ont montré une résistance à la « gentamicine, à l’amikacine et à la ciproflaxine » ainsi qu’une résistance aux antibiotiques bêta-lactamines. Certaines des bactéries n’avaient qu’une seule copie du plasmide, cependant, d’autres en avaient jusqu’à treize. Une corrélation a été observée avec le nombre de copies du gène et la résistance aux antibiotiques. Les auteurs de l’étude ont estimé que l’utilisation d’antibiotiques exerçait une pression sélective sur les bactéries et que les plasmides codaient souvent pour des résistances multiples., Ainsi, les bactéries sélectionnées ont non seulement une résistance à l’antibiotique utilisé, mais également à d’éventuels autres antibiotiques non apparentés. Les résultats de cette recherche laissent espérer que des recherches continues seront menées pour analyser l’importance de ces plasmides ESBL (20).
Une étude de cas récente a étudié cinq isolats d’E. aerogenes présentant une résistance aux β-lactamines et aux fluoroquinolones pendant le traitement d’un patient ayant subi une revascularisation myocardique., Le patient a reçu des antibiotiques à large spectre, y compris l’imipénème et la polymyxine, donnant ainsi naissance à des mutants résistants à L’imipénème et à la polymyxine d’E. aerogenes en raison de modifications de la synthèse de la porine et de l’équilibre du LPS. Cinq isolats de ces souches résistantes appelées A, B,C, D et E ont été comparés à L’aide de PFGE (Pulse-Field Gel Electrophoresis) au brin parental ATCC13048., Une corrélation a été rapportée entre les isolats avec la présence D’Omp36 codant pour la synthèse de la porine observée dans l’isolat A, et ceux qui avaient le gène OmpX qui a régulé l’expression de la porine (isolats B et C) de sorte que les isolats avec OmpX conféraient une résistance à l’impénème. Des études antérieures ont montré que les modifications du LPS ont contribué à la résistance aux antibiotiques. Ces résultats montrent que le gène OmpA responsable des modifications du LPS était présent dans les cinq isolats, y compris le brin parental ATCC13048., Les isolats D et E ont montré des écarts dans L’équilibre du LPS par rapport à ATCC13048, provoquant une résistance à la colistine peu de temps après l’administration. Étant donné que les profils PFGE des cinq isolats montrent une similitude, les chercheurs ont suggéré que les isolats B à E sont des variantes de l’isolat A, résultant en réponse à des antibiotiques administrés au patient pendant la période de traitement (22).
les Autres membres du même genre
Nous avons trouvé un article intéressant sur la bactérie Enterobacter cloacae. Cet article parle D’Enterobacter cloacae et de sa résistance aux céphalosporines de troisième génération., Les céphalosporines appartiennent à la classe des antibiotiques B-lactamines et ce type d’antibiotiques inhibe la synthèse de la paroi cellulaire bactérienne. Les B-lactames se lient de manière covalente aux enzymes de la transpeptidase et les inactivent (responsables de la réticulation de l’acide aminé qui forme la couche de peptidoglycane de la paroi cellulaire). Étant donné que l’enzyme transpeptidase est maintenant inactivée par l’antibiotique et que la paroi cellulaire ne peut plus former de réticulations, la cellule finira par éclater et lyser, tuant ainsi les bactéries. Cependant, les bactéries ont développé différents types de résistance aux antibiotiques., Par exemple, l’enzyme B-lactamase sert à hydrolyser et à briser les anneaux B-lactame des antibiotiques et annule donc les effets des antibiotiques. Cet article montre que la recherche montre que la B-Lactamase D’Enterobacter cloacae joue un rôle différent. Ils n’hydrolysent pas les anneaux de B-lactame. Au lieu de cela, la résistance D’Enterobacter cloacae aux céphalosporines provient d’une mutation due à la production constitutive de B-Lactamases., L’article conclut qu’après de nombreuses expériences, le mécanisme de résistance D’Enterobacter cloacae reste à déterminer, mais il est un fait qu’il n’y a pas d’hydrolyse du cycle B-lactame et qu’une sorte de mutation est à l’origine de la prévention de la liaison du médicament à l’enzyme ou qu’il existe une sorte de barrière de perméation responsable de la résistance.
Source d’Énergie
l’Un des sous-produits de la fermentation est de l’hydrogène., La capacité D’Enterobacter aerogenes à produire de l’hydrogène par la fermentation d’une variété de sucres, y compris le glucose, le galactose, le fructose, le mannose, le mannitol, le saccharose, le maltose et le lactose, a conduit les scientifiques à étudier l’utilisation du métabolisme de cette bactérie comme moyen d’acquérir de l’énergie propre. De nombreuses bactéries peuvent produire de l’hydrogène par fermentation à un pH neutre, et E. aerogenes ne fait pas exception. Son pH optimal pour la production d’hydrogène est compris entre 6 et 7., Cependant, il est difficile de maintenir ce pH élevé pendant la fermentation, car le processus donne des produits acides tels que l’acide acétique, l’acide succinique et l’acide lactique, et l’accumulation de ces produits entraîne une diminution du pH. généralement, les bactéries cessent la fermentation et cessent donc la production d’hydrogène à des niveaux de pH aussi faibles. Cependant, une souche D’E. aerogenes, HO-39, a la capacité de continuer la fermentation à des niveaux de pH aussi bas que 4., Cette qualité rend la souche HO-39 souhaitable comme source d’énergie car elle continuera la production d’énergie sans trop de régulation de l’environnement bactérien. Lorsque la fermentation bactérienne est inhibée à des niveaux de pH bas, l’alcali doit continuellement être ajouté à la culture bactérienne afin de contrer le faible pH causé par l’accumulation des acides organiques. L’alcali est cher et, par conséquent, n’est pas rentable pour l’exploitation de l’énergie. L’utilisation d’un anaérobe facultatif acidurique tel que E. aerogenes réduira la quantité d’alcali nécessaire au maintien de la production d’hydrogène., Ainsi, cette bactérie pourrait être utilisée comme source d’énergie propre rentable (17).
2. Lederberg, Josué; Martin Alexandre . Encyclopédie de microbiologie. 2e ed. San Diego, Californie.: Academic Press, 2000
3. Sankaran, Neeraja. Les Microbes et les gens un A-Z de micro-organismes dans nos vies. Phoenix, Az.: Oryx Press, 2000
5. Collins, C. G.; P. M. Lune, J. M. Grange, J. O Falkinham III. Méthodes Microbiologiques. 8e ed. Londres: Arnold, 2004
7. Greenwood, David; Richard C. B. Slack; John F. Peuthere., Microbiologie médicale, Guide des Infections microbiennes: agents pathogènes, immunité, diagnostic et contrôle en laboratoire. Edimbourg: Churchill Livingstone, 2002
9. Janda, J. Michael; Sharon L. Abbott. Les entérobactéries 2e éd. Washington: ASM press, 2006
11. Bailey, W. R. et E. G. Scott. Microbiologie diagnostique, 4e éd. Saint-Louis, Mo.: Le C. V. Mosby Co. De 1974
12. De Gheldre, Y. . Enquêtes épidémiologiques nationales sur Enterobacter aerogenes dans les hôpitaux belges de 1996 à 1998. J Clin Microbiol. 2001 Mars 39 (3): 889-896
13. Fraser, Susan L. MD, . Infections À Entérobactéries., eMedicine. 2007 Jan.
14. Rhondina, Matthieu T. . Aortite abdominale due à Streptococcus pneumoniae et Enterobacter aerogenes un rapport de cas et un examen. J Gen Intern Med. 2006 Juillet; 21 (7): C1–C3.
16. Kumar Mohan Nair, Monoj . Clonage et séquençage du gène ompA D’Enterobacter sakazakii et Développement D’une PCR ciblée par ompA pour la détection rapide D’Enterobacter sakazakii dans les préparations pour nourrissons. Appl Environ Microbiol. 2006 avril; 72 (4): 2539-2546.
17. Yokoi, Haruhiko, et coll. « Les caractéristiques de la Production d’Hydrogène par Aciduric Enterobacter aerogenes Souche HO-39.,” Journal de la Fermentation et de la bio-ingénierie Vol. 80 No 6 (1995): 571 à 574. Imprimer.
19. Thiolas, Aurélie, Claude Bollet, émergence Successive de souches D’Enterobacter aerogenes résistantes à L’imipénème et à la colistine chez un Patient. Les Agents antimicrobiens et la Chimiothérapie, avril 2005; 49 (4): 1354-1358.
20. Sharma J, Ray P, Sharma M. profil Plasmidique de BLSE la production de bactéries Gram-négatives et la corrélation avec la sensibilité aux ß-lactamines médicaments. Indian J Pathol Microbiol 2010;53:83-6
21.,A H Seeberg, R M Tolxdorff-Neutzling et B Wiedemann les bêta-lactamases chromosomiques D’Enterobacter cloacae sont responsables de la résistance aux céphalosporines de troisième génération.Antimicrob. Les Agents Chemother., Jun 1983; 23: 918-925.
22. Thiolas, Aurélie, Claude Bollet, émergence Successive de souches D’Enterobacter aerogenes résistantes à L’imipénème et à la colistine chez un Patient. Les Agents antimicrobiens et la Chimiothérapie, avril 2005; 49 (4): 1354-1358.
certaines parties de cette page ont été créées par Tiffany M. Liu, une étudiante du Professeur Rachel Larsen à L’Université de Californie à San Diego.,
Edité par Paul Erpelo / Salvatore Grasso / Everardo Mojica/ Joseph Truong et Frank Wolf/ Kimberly Klages et Sandra Montes / Daisy Mendez étudiants de M Glogowski à L’Université Loyola