objectifs D’apprentissage
- énoncez la règle de Hund.
- appliquer la règle de Hund au remplissage des orbitales.
- utilisez des diagrammes de remplissage orbital pour décrire l’emplacement des électrons dans un atome.
vous êtes-vous déjà demandé ce que signifient ces signes de limite de charge sur un pont?
Le panneau ci-dessus indique que rien de plus de cinq tonnes n’est autorisé car cela endommagera la structure., Il y a des limites à la quantité de poids qu’un pont peut supporter, il y a des limites au nombre de personnes qui peuvent occuper une pièce en toute sécurité, et il y a des limites à ce qui peut entrer dans une orbitale électronique.

règle de Hund
la dernière des trois règles pour construire des arrangements d’électrons exige que les électrons soient placés un à la fois dans un ensemble d’orbitales dans le même sous-niveau. Cela minimise les forces répulsives naturelles qu’un électron a pour un autre., La règle de Hund stipule que les orbitales d’énergie égale sont chacune occupées par un électron avant que toute orbitale ne soit occupée par un deuxième électron et que chacun des électrons uniques doit avoir le même spin. La Figure ci-dessous montre comment un ensemble de trois orbitales p est rempli avec un, deux, trois, et quatre électrons.
diagrammes de remplissage Orbital
un diagramme de remplissage orbital est la façon la plus visuelle de représenter la disposition de tous les électrons dans un atome particulier., Dans un diagramme de remplissage orbital, les orbitales individuelles sont représentées sous forme de cercles (ou de carrés) et les orbitales d’un sous-niveau sont dessinées l’une à côté de l’autre horizontalement. Chaque sous-niveau est marqué par son niveau d’énergie principal et son sous-niveau. Les électrons sont indiqués par des flèches à l’intérieur des cercles. Une flèche pointant vers le haut indique une direction de rotation, tandis qu’une flèche pointant vers le bas indique une autre direction. Les diagrammes de remplissage orbital pour l’hydrogène, l’hélium et le lithium sont présentés dans la Figure ci-dessous.
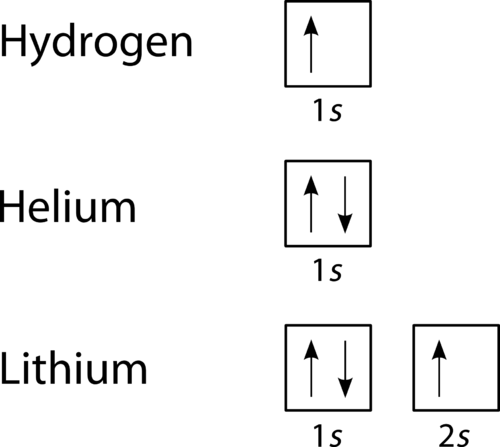
la Figure 2., Diagrammes de remplissage Orbital pour l’hydrogène, l’hélium et le lithium.
selon le processus D’Aufbau, les sous-niveaux et les orbitales sont remplis d’électrons par ordre croissant d’énergie. Étant donné que le sous-niveau s se compose d’une seule orbitale, le deuxième électron se couple simplement avec le premier électron comme dans l’hélium. L’élément suivant est le lithium et nécessite l’utilisation du sous-niveau disponible suivant, le 2s.
le schéma de remplissage pour le carbone est illustré dans la Figure ci-dessous. Il y a deux électrons 2 p pour le carbone et chacun occupe sa propre orbitale 2 p.,
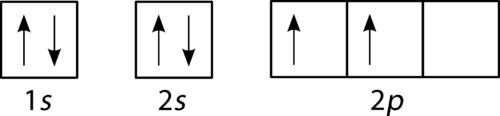
la Figure 3. Diagramme de remplissage Orbital pour le carbone.
Oxygène a quatre 2 p électrons. Après que chaque orbitale 2 p ait un électron, le quatrième électron peut être placé dans la première orbitale 2 p avec un spin opposé à celui de l’autre électron dans cette orbitale.
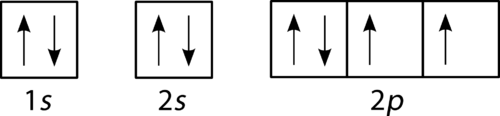
la Figure 4. Diagramme de remplissage Orbital pour l’oxygène.
Résumé
- Hund règle spécifie l’ordre de l’électron de remplissage à l’intérieur d’un ensemble d’orbitales.,
- Les diagrammes de remplissage Orbital sont un moyen d’indiquer les emplacements des électrons dans les orbitales.
Pratique
Utiliser le lien ci-dessous pour effectuer l’exercice suivant:
https://www.caymanchem.com/app/template/chemAssistant,Outil.VM/itemid/4001
- sélectionnez un atome dans la liste (vous voudrez probablement faire des nombres atomiques inférieurs). Laissez le nombre définir un zéro.
- recherchez l’atome sur un tableau périodique et déterminez le nombre d’électrons présents.
- dessinez le diagramme de remplissage orbital de l’atome.,
- Cliquez sur le bouton « Calculer”, et comparez votre réponse avec celle prévue.
Examen
- l’État de la règle de Hund.
- Qu’est-ce qu’un diagramme de remplissage orbital?
- Le diagramme de la Figure ci-dessous est-il correct? Expliquez votre réponse.

- Est le schéma de la Figure ci-dessous correct? Expliquez votre réponse.,

Glossaire
- règle de Hund: les orbitales d’énergie égale sont chacune occupées par un électron avant que toute orbitale ne soit occupée par un second électron et que chacun des électrons doit avoir le même spin.
- diagramme de remplissage orbital: une façon visuelle de représenter la disposition de tous les électrons dans un atome particulier.