Poikkeus 2: Puutteellinen Tavua
toinen poikkeus Oktetti Sääntö on, kun on liian vähän valence elektroneja, joka johtaa epätäydellinen Oktetti. On vielä useampia tilanteita, joissa oktettisääntö ei anna kaikkein oikeaoppisinta kuvausta molekyylistä tai ionista. Näin on myös keskeneräisten oktettien kohdalla. Laji puutteellisia tavujen ovat melko harvinaisia ja yleensä löytyy vain joitakin beryllium -, alumiini -, ja boorin yhdisteitä, mukaan lukien boori hydridit., Katsotaanpa yksi tällainen hydridi, \(BH_3\) (Borane).
Jos yksi oli tehdä Lewis rakenne \(BH_3\) seuraavat perus strategioita piirustus Lewis rakenteita, voisi varmaan keksiä tätä rakennetta (Kuva 3):
ongelmana tässä rakenteessa on, että boori on epätäydellinen oktetti; se vain on kuusi elektronia sen ympärille., Vetyatomit voivat luonnollisesti vain on vain 2 elektronia niiden uloin kuori (versio oktetti), ja sinänsä ei ole mitään vapaa-elektronit muodostavat kaksoissidoksen, jossa booria. Voisi otaksua, että epäonnistuminen tämä rakenne muodostaa täydellinen tavujen täytyy tarkoittaa, että tämä side pitäisi olla ionic sijaan kovalenttinen., Kuitenkin, boori on elektronegatiivisuus, joka on hyvin samanlainen kuin vety, eli siellä on todennäköisesti hyvin vähän ioninen luonne vedyn booria joukkovelkakirjoja, ja sellaisenaan tämä Lewis rakenne, vaikka se ei täytä oktetti sääntö on todennäköisesti paras rakenne mahdollista kuvaa BH3 Lewisin teoria. BH3: n epätäydellisen oktetin voi selittää muun muassa sillä, että se on yleisesti ohimenevä laji, joka muodostuu tilapäisesti reaktioissa, joihin liittyy useita vaiheita.
katsotaanpa katsomaan toinen epätäydellinen oktetti tilanne tekemisissä boori, BF3 (Boori trifluorine)., Kuten BH3, alkuperäinen piirustus Lewis rakenne BF3 muodostaa rakenne, jossa boori on vain kuusi elektronia sen ympärille (Kuva 4).
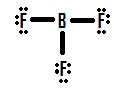
Jos et katso Kuva 4, voit nähdä, että fluoriatomia hallussaan ylimääräistä yksinäinen paria, että he voivat käyttää tehdä lisää joukkovelkakirjoja boori, ja saatat ajatella, että kaikki sinun täytyy tehdä, on tehdä yksi yksinäinen pari bond ja rakenne on oikea., Jos lisäämme yksi kaksoissidos välillä boori ja yksi fluorines saamme seuraavat Lewis Rakenne (Kuva 5):
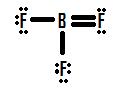
Jokainen fluoria on kahdeksan elektronia, ja boorin atomin on kahdeksan samoin! Jokaisella atomilla on täydellinen oktetti. Ei niin nopeasti. Meidän on tutkittava tämän rakenteen muodolliset syytökset. Fluori, joka jakaa double side boori on kuusi elektronia sen ympärille (neljä sen kaksi yksinäistä paria elektroneja ja yksi kunkin sen kaksi joukkovelkakirjojen boori)., Tämä on yksi vähemmän electron kuin määrä valence elektroneja, se olisi luonnollisesti (Ryhmä seitsemän elementtejä on seitsemän valence elektroneja), niin se on virallisen syytteen +1. Kaksi flourines, jotka jakavat yhden joukkovelkakirjat boori on seitsemän elektronia ympärille (kuusi niiden kolmen yksinäinen paria ja yksi yhden joukkovelkakirjat boori). Tämä on sama määrä kuin määrä valence elektronit he olisivat omasta, joten ne molemmat on muodollinen maksu on nolla. Lopuksi boorilla on ympärillään neljä elektronia (yksi jokaisesta sen neljästä fluorin kanssa jaetusta sidoksesta)., Tämä on yksi elektroni kuin määrä valence elektroneja, jotka boori olisi oma, ja sellaisena boori on muodollinen vastaa -1.
Tämä rakenne tukee se, että kokeellisesti määritetty bond pituus boori, fluoria joukkovelkakirjojen BF3 on vähemmän kuin mitä olisi tyypillinen yhden siteen (ks Bond Järjestyksen ja Pituudet)., Kuitenkin, tämä rakenne on ristiriidassa yksi suurimmista sääntöjen muodollinen maksut: Negatiivinen muodollisia syytteitä pitäisi löytyä enemmän electronegative atomin(t) bond, mutta rakenne on kuvattu Kuvassa 5, positiivinen muodollinen maksu on löydetty fluoria, joka ei vain on kaikkein electronegative elementin rakenne, mutta kaikkein electronegative osa koko jaksollisen (\(\chi=4.0\)). Boori toisaalta, kanssa paljon pienempi elektronegatiivisuus 2.0, on negatiivinen virallista syytettä tässä rakenteessa., Tämä muodollinen varaus-elektronegatiivisuus erimielisyys tekee tämän kaksoissidoksisen rakenteen mahdottomaksi.
Kuitenkin suuri elektronegatiivisuus ero täällä, toisin kuin vuonna BH3, merkitsee huomattavaa polar joukkovelkakirjojen välillä boori ja fluori, mikä tarkoittaa, että on korkea ioninen luonne tämän molekyylin. Tämä viittaa siihen mahdollisuus semi-ionisia, kuten nähdään Kuvassa 6:

Mikään näistä kolmesta rakenteita on ”oikea” rakenne tässä tapauksessa., Useimmat ”oikea” rakenne on todennäköisesti resonanssi kaikki kolme osaa: yksi epätäydellinen oktetti (Kuva 4), yksi kaksoissidos (Kuva 5), ja yksi kanssa ionic bond (Kuva 6). Eniten edistää rakenne on luultavasti puutteellinen oktetti rakenne (koska Kuvassa 5 on käytännössä mahdotonta ja Luku 6 ei vastaa ylös käyttäytymistä ja ominaisuuksia BF3). Kuten näette silloinkin, kun muita mahdollisuuksia on, epätäydelliset oktetit voivat parhaiten kuvata molekyylirakennetta.,
sivuhuomautuksena, se on tärkeää huomata, että BF3 usein joukkovelkakirjalainoja F – ion jotta voidaan muodostaa BF4 – pikemminkin kuin pysyä kuin BF3. Tämä rakenne täydentää boorin oktettia ja se on yleisempi luonnossa. Tämä on esimerkki siitä, että epätäydellinen tavujen ovat harvinaisia, ja muut kokoonpanot ovat yleensä edullisempia, kuten liimaus muita ioneja kuten BF3 .
Esimerkki: \(BF_3\)
Piirrä Lewis rakenne boori trifluoride (BF3).
liuos
1. Lisää elektroneja (3*7) + 3 = 24
2., Draw-luvulla:
3. Lisää tavujen ulko-atomeja:
4. Lisätä ylimääräisiä elektroneja (24-24=0) keski-atom:
5. Onko keskuselektronilla octet?
- ei. Se on 6 elektronia
- Lisätä useita bond (kaksoissidos) nähdä, jos keski-atomi voi saavuttaa oktetti:
6. Keskiboronilla on nyt oktetti (resonanssissa olisi kolme Lewis-rakennetta)
kuitenkin…,
- tässä rakenteessa kaksoissidoksella fluoriatomi jakaa ylimääräisiä elektroneja boorin kanssa.
- fluori olisi ’+’ osittainen maksu, ja boori-a ’-’ osittainen maksu, tämä on ristiriidassa electronegativities fluoria ja booria.
- Siten, rakenne BF3, yhden joukkovelkakirjoja, ja 6 valence elektroneja ympäri keski boori on todennäköisesti rakenne
- BF3 reagoi voimakkaasti kanssa yhdisteitä, joilla on jakamaton pari elektroneja, jotka voidaan muodostaa side boori: