| PITKÄN AIKAVÄLIN VOIMISTUMISTA |
|
Pitkän aikavälin voimistumista (LTP) on prosessi, jossa synapsit vahvistuvat. Siitä on tehty paljon tutkimusta, koska sillä on todennäköinen rooli monenlaisessa muistissa. LTP on pitkäaikaisen masennuksen vastakohta (LTD). LTP: ssä presynaptisen neuronin voimakkaan stimulaation jälkeen synaptisen neuronin vasteen amplitudi kasvaa., Ärsyke käytetään yleensä lyhytkestoisia (alle 1 sekunti), mutta korkea taajuus (yli 100 Hz). Vuonna postsynaptisten hermopäätteiden, tämä ärsyke aiheuttaa riittävä depolarisaatio evakuoida magnesium-ionit, jotka ovat estää NMDA-reseptoria, jolloin suuria määriä kalsium-ioneja tulla dendriitin.
nämä kalsiumionit ovat erittäin tärkeitä solunsisäisiä sanansaattajia, jotka aktivoivat monia entsyymejä muuttamalla niiden konformaatiota. Yksi näistä entsyymeistä on kalmoduliini, joka aktivoituu, kun siihen sitoutuu neljä kalsiumionia., Sen jälkeen siitä tulee CA2+/calmodulin, LTP: n tärkein toinen viestinviejä. Ca2+/calmodulin sitten puolestaan aktivoi muita entsyymejä, jotka pelaavat keskeinen rooli tässä prosessissa, kuten adenylaattisyklaasia ja Ca2+/calmodulin-dependent protein kinase II (CaM kinaasi II). Nämä entsyymit puolestaan muokkaavat muiden molekyylien avaruudellista konformaatiota, yleensä lisäämällä niihin fosfaatti-ionin. Tätä yleistä katalyyttistä prosessia kutsutaan fosforylaatioksi.,
|
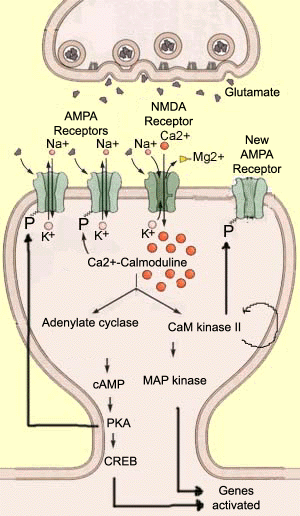
Näin ollen aktivoitu adenylaattisyklaasia valmistaa syklinen adenosiini mono-fosfaatti (cAMP), joka puolestaan katalysoi toimintaa toisen proteiini kinaasi A (tai PKA). Toisin sanoen on tyypillinen biokemiallisten reaktioiden kaskadi, jolla voi olla monia erilaisia vaikutuksia. esimerkiksi, PKA phosphorylates AMPA-reseptoreihin, jolloin ne pysyvät auki pidempään, kun glutamaatti sitoutuu niihin. Tämän seurauksena postsynaptinen neuroni depolarisoituu entisestään, mikä edistää LTP: tä., muut kokeet ovat osoittaneet, että KREBIPROTEIINI on toinen PKA: n kohde. CREB on merkittävä rooli geenien transkriptio, ja sen aktivointi johtaa uusien AMPA-reseptoreihin, jotka voivat lisätä synaptic tehokkuutta entisestään. toinen entsyymi aktivoituu Ca2+/calmodulin, Nokka-kinaasi II, on ominaisuus, joka on ratkaiseva pysyvyys LTP: se voi fosforyloida itse! Sen entsymaattinen aktiivisuus jatkuu kauan sen jälkeen, kun kalsiumia on evakuoitu solusta ja Ca2+/calmodulin on poistettu käytöstä., CaM-kinaasi II voi sitten puolestaan fosforyloida AMPA ja luultavasti myös muita proteiineja, kuten MAP-kinaasit, jotka ovat mukana rakentamisessa dendrites, tai NMDA-reseptorien itse, jonka kalsiumia johtokyky olisi kasvanut tämän fosforylaation. |
 |
antaa jonkinlaisen käsityksen monimutkaisuus aineenvaihdunnan sekvenssit vastuussa LTP, me mainita kolme muuta entsyymejä tällä hetkellä tutkitaan., Proteiinikinaasi C (PKC) näkyy fosfory-AMPA samassa paikassa kuin CaM-kinaasi II. – Inhibiittori 1 (ou I1) näyttää olevan aktivoitu PKA ja estää fosfataasi 1 dephosphorylating AMPA reseptoreihin. Ja tyrosiinikinaasi SRC voi aktivoitua suoraan AMPA-reseptoreista ja fosforyloida sitten NMDA-reseptorit.,
|
lisäksi kaikki post-synaptisen mekanismeista perustaminen LTP, se on pitkään oletettu, että jotkut presynaptinen muutokset tapahtuvat aikana seurannut ylläpitovaiheeseen. Mutta tiettyjä muutoksia, kuten lisätä määrä glutamaattia vapautuu presynaptisen hermosolun, merkitsisi läsnäolo taaksepäin messenger, joka menee takaisin tämä neuroni ja muokkaa sitä., Koska typpioksidi (NO) on kaasua sen luonnollisessa tilassa, ja voi siten hajanainen solukalvojen läpi, se olisi ihanteellinen ehdokas tähän rooliin. Sen osallistumisesta käydään silti paljon keskustelua ja kiistaa.