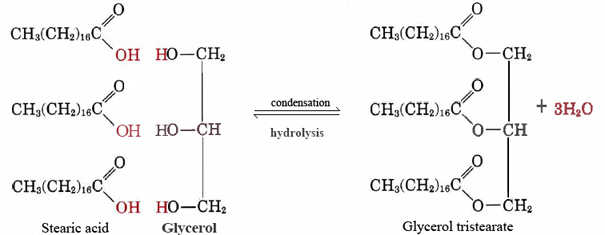
hyvä esimerkki ei-polaarisia lipidejä on neutraali rasva glyseroli tristearate. Tämä yleisin eläinrasvan muoto toimii energian varastona ja eristeenä lämmönhukkaa vastaan. Molekyylitasolla se on rakennettu kolmesta molekyylien steariinihappo ja yksi glyseroli:
 (1)
(1)
monet ei-polaarisia lipidejä voidaan tehdä yhdistämällä eri pitkäketjuiset rasvahapot glyseroli., Koska nämä hapot olivat alun perin peräisin rasvoista, niistä käytetään yhteisnimitystä rasvahapot.
Huomaa, että kunkin steariini-tai muiden rasvahappojen molekyyli, joka yhdistää yksi —OH-ryhmät glyserolia, molekyyli vettä on annettu pois, ja niin reaktio on tiivistymistä. On käynyt ilmi, että hyvin monet tärkeät Biologiset molekyylit kootaan kondensaatioreaktioilla, joiden aikana vettä vapautuu. Eq: n kääntöpuoli. (1), jossa vesi reagoi suuren molekyylin kanssa ja jakaa sen pienemmiksi kappaleiksi, kutsutaan hydrolyysiksi., Hydrolyysin avulla elävät organismit voivat hajottaa muiden lajien valmistamia molekyylejä. Näin saatavat yksinkertaiset rakennuspalikat voidaan sitten rekombinoida tiivistymisreaktioilla muodostamaan uuteen isäntäänsä sopivia rakenteita.
toisin kuin glyseroli tristearate löytyy eläimiä, kasvirasvat sisältävät useita kaksoissidoksia niiden pitkiä hiilivetyketjuja. Tämä polyunsaturation esittelee ”kinks” in hiilivetyketjuja, koska esteen kierto ja 120 asteen kulmat, jotka liittyvät kaksoissidoksia., Näin ollen se on vaikeampi kohdistaa ketjut rinnakkain (ks. Luku \(\PageIndex{1}\) ), ja tyydyttymättömiä rasvoja, älä pakkaa yhteen niin helposti kidehilan. Kuten alkaaneilla, myös ketjun pituus määrittää, onko rasva nestemäistä vai kiinteää ja missä sulamispiste tapahtuu.
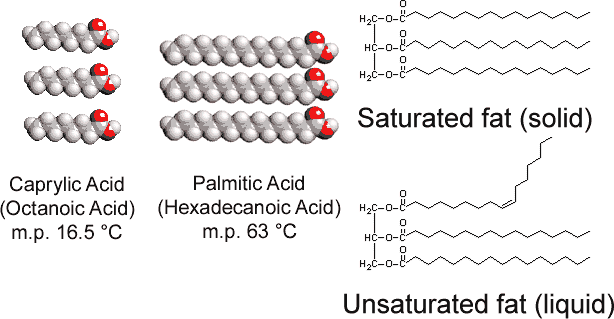
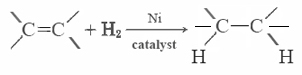
Eniten tyydyttymättömiä rasvoja (kuten maissiöljy) ovat nesteitä tavallisille lämpötiloissa, kun taas tyydyttyneitä rasvoja (voita) ovat kiinteitä. Kasviöljyt voidaan muuntaa hydraamalla yhdisteiksi, jotka ovat kiinteitä aineita. Tämä prosessi liittyy lisäämällä H2 katalyyttisesti double bonds:
Hydrolyysi rasvoja on tärkeää valmistuksessa saippuat., Se voidaan nopeuttaa lisäämällä vahva pohja, kuten NaOH tai KOH, jolloin reaktio on nimeltään saippuointi. Koska saippuointi edellyttää, että pH reaktio seos on korkea, rasvahappo, joka on valmistettu tulee erottaa sen anioni. Kun glyserolitristearaattia saponifioidaan esimerkiksi NaOH: n kanssa, muodostuu natriumstearaattia, joka on suhteellisen Vesiliukoinen aine ja yleinen saippua.
kyky saippuat puhdistaa rasvasta ja öljystä likaantuneiden pintojen on seurausta dual hydrofobinen-hydrofiilinen rakenteita niiden molekyylejä., Esimerkiksi stearaatti-ioni koostuu pitkästä ei-polaarisesta hiilivetyketjusta, jonka toisessa päässä on erittäin polaarinen KOO-ryhmä.
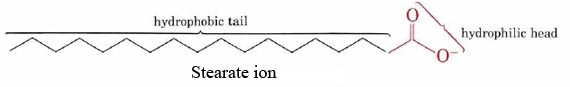
hydrofobinen hiilivety-ketju yrittää välttää kosketusta vesipitoiset media, kun taas anioninen ryhmä helposti mahtuu dipoli nähtävyyksiä ja vetysidoksia vesimolekyylien.
kaksi tapaa, että hydrofobisia osia stearate ionit voivat välttää veden klusterin yhdessä pinnalla tai liuotetaan pieni määrä öljyä tai rasvaa (ks. Luku \(\PageIndex{2}\) ).,
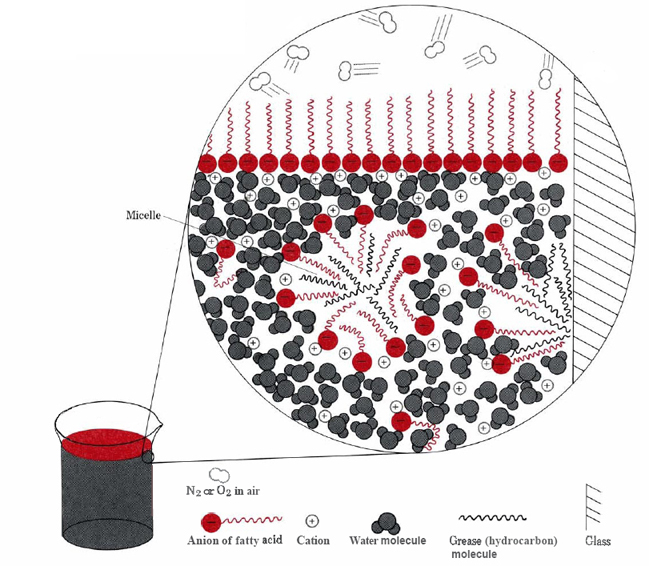
jälkimmäisessä tapauksessa hydrofiiliset päät saippua molekyylit yhteyttä veden ulkopuolella rasvan, muodostaen rakenne tunnetaan misellin. Koska outsides misellien ovat negatiivisesti varautuneita, ne hylkivät toisiaan ja estää rasvaa pisaroita yhdistymisestä., Siksi rasva suspendoidaan (emulgoidaan) veteen ja se voidaan pestä pois helposti.
Luonnolliset saippuat, kuten natriumstearaatti, valmistettiin alun perin kotona kuumentamalla eläinrasvaa puuntuhkalla, joka sisälsi potaskaa, K2CO3: ta. Suuria määriä tuotetaan edelleen teollisesti, mutta melkoisesti saippuat on korvattu pesuaineilla. Tämä on seurausta saippuoiden epätoivotusta käyttäytymisestä kovassa vedessä. Kalsium, magnesium ja muut kovan veden kationit muodostavat liukenemattomia yhdisteitä yhdistettynä rasvahappojen anioneihin., Tämä tuottaa likaisella saostuu ja estää saippua molekyylit emulgoivat rasvaa, ellei suuri ylimäärä käytetään.
Pesuaineita, kuten alkylbenzenesulfonates (ABS) ja lineaarinen alkylbenzenesulfonates (LAS) rakenteet ovat hyvin samankaltaisia natrium stearate, paitsi että täyteen ryhmään niiden hydrofiiliset päät on —SO3– kiinnitetty bentseeni rengas. ABS-pesuaineissa on myös metyyli (CH3) – ryhmiä, jotka haarautuvat hiilivetyketjuistaan.,
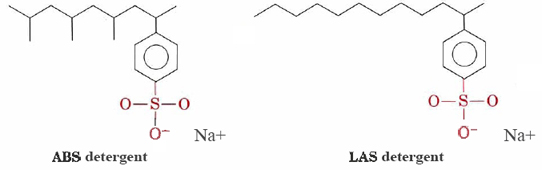
Tällaiset molekyylit eivät sakka kovan veden kationeja ja siksi ovat enemmän sopii konepesuun vaatteita. LAS-pesuaineet korvasivat ABS: t 1960-luvun puolivälissä, kun havaittiin, että jälkimmäiset eivät olleet biohajoavia. Ne saivat joet ja jopa vesijohtoveden peittymään pesuainesudeilla ja vaahdolla. Ilmeisesti mikro-organismien entsyymit, jotka olivat kehittyneet hajottamaan luonnollisten rasvojen ja rasvahappojen muodostamattomia hiilivetyketjuja, eivät kyenneet sulattamaan ABS-molekyylien haarautuneita ketjuja., Vaikka Las-pesuaineet ovat ihmisen valmistamia, ne jäljittelevät luonnossa esiintyvien molekyylien rakenteita ja ovat biohajoavia.