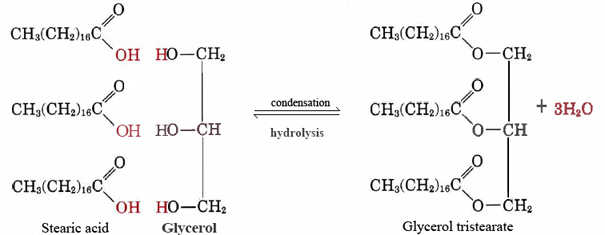
un buen ejemplo de un lípido no polar es el triestearato de glicerol de grasa neutra. Esta forma más común de grasa animal sirve como almacén de energía y como aislamiento contra la pérdida de calor. A nivel molecular se construye a partir de tres moléculas de ácido esteárico y una de glicerol:
 (1)
(1)
se pueden hacer muchos lípidos no polares combinando diferentes ácidos de cadena larga con glicerol., Debido a que estos ácidos se derivaron originalmente de las grasas, se les conoce colectivamente como ácidos grasos.
observe que por cada molécula de ácido esteárico u otra molécula de ácido graso que se combina con uno de los grupos —OH de glicerol, se emite una molécula de agua, por lo que la reacción es una condensación. Resulta que muchas moléculas biológicas importantes se juntan por reacciones de condensación durante las cuales se emite agua. El reverso de la EC. (1), en el que el agua reacciona con una molécula grande y la divide en trozos más pequeños, se llama hidrólisis., Al llevar a cabo la hidrólisis, los organismos vivos pueden descomponer las moléculas fabricadas por otras especies. Los bloques de construcción simples obtenidos de esta manera pueden recombinarse por reacciones de condensación para formar estructuras apropiadas para su nuevo huésped.
en contraste con el triestearato de glicerol que se encuentra en los animales, las grasas vegetales contienen numerosos enlaces dobles en sus largas cadenas de hidrocarburos. Esta poliinsaturación introduce «torceduras» en las cadenas de hidrocarburos debido a la barrera a la rotación y los ángulos de 120° asociados con los dobles enlaces., En consecuencia, es más difícil alinear las cadenas laterales por lado (ver Figura \(\PageIndex{1}\) ), y las grasas insaturadas no pack tan fácilmente en una red cristalina. Como ocurrió con los alcanos, la longitud de la cadena también determina si una grasa es líquida o sólida, y dónde se produce el punto de fusión.
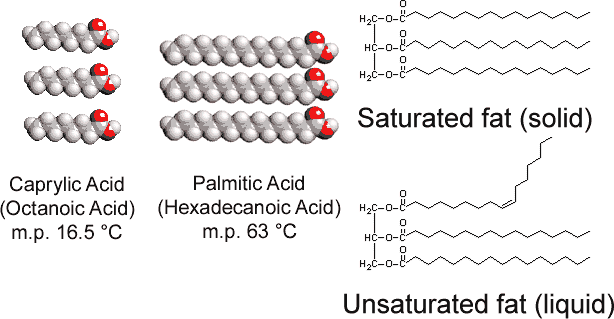
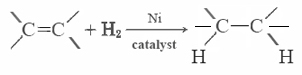
La mayoría de las grasas insaturadas (como el aceite de maíz) son líquidos a temperaturas normales, mientras que las grasas saturadas (como la mantequilla) son sólidas. Los aceites vegetales se pueden convertir por hidrogenación en compuestos que son sólidos. Este proceso implica añadir H2 catalíticamente a los dobles enlaces:
la hidrólisis de grasas es importante en la fabricación de jabones., Se puede acelerar mediante la adición de una base fuerte como NaOH o KOH, en cuyo caso la reacción se llama saponificación. Dado que la saponificación requiere que el pH de la mezcla de reacción sea alto, el ácido graso que se produce se disociará a su anión. Cuando el triestearato de glicerol se saponifica con NaOH, por ejemplo, se forma estearato de sodio, una sustancia relativamente soluble en agua y un jabón común.
la capacidad de los jabones para limpiar la grasa y el aceite de superficies sucias es el resultado de las estructuras hidrofóbicas e hidrofílicas duales de sus moléculas., El ion estearato, por ejemplo, consiste en una larga cadena de hidrocarburos no polares con un grupo COO altamente polar en un extremo.
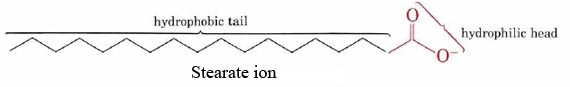
la cadena hidrofóbica de hidrocarburos intenta evitar el contacto con medios acuosos, mientras que el grupo aniónico acomoda fácilmente las atracciones dipolares y los enlaces de hidrógeno de las moléculas de agua.
las dos formas principales en que las porciones hidrofóbicas de iones de estearato pueden evitar el agua son agruparse en la superficie o disolverse en una pequeña cantidad de aceite o grasa (ver figura \(\PageIndex{2}\) ).,
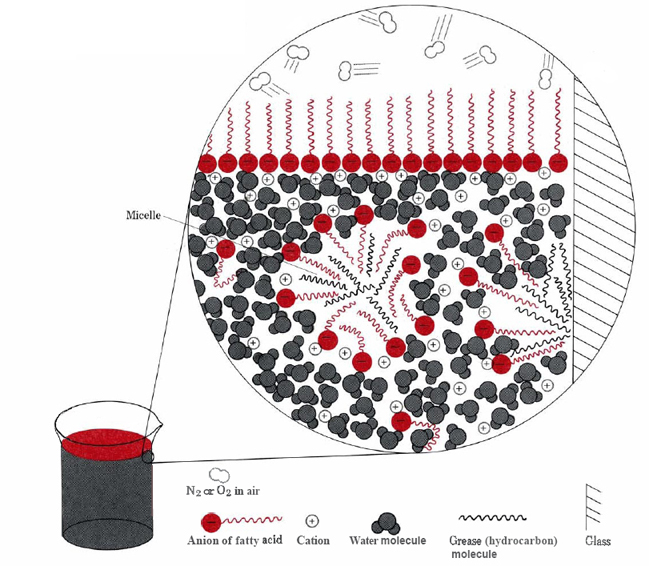
en este último caso, las cabezas hidrofílicas de las moléculas de jabón entran en contacto con el agua fuera de la grasa, formando una estructura conocida como micela. Dado que las partes exteriores de las micelas están cargadas negativamente, se repelen entre sí y evitan que las gotitas de grasa se recombinen., Por lo tanto, la grasa se suspende (emulsiona) en el agua y se puede lavar fácilmente.
los jabones naturales, como el estearato de sodio, se fabricaban originalmente en el hogar calentando grasa animal con cenizas de madera, que contenían potasa, K2CO3. Todavía se producen grandes cantidades industrialmente, pero en gran medida los jabones han sido sustituidos por detergentes. Esto es una consecuencia del comportamiento indeseable de los jabones en agua dura. El calcio, el magnesio y otros cationes de agua dura forman compuestos insolubles cuando se combinan con los aniones de los ácidos grasos., Esto produce precipitados espumosos y evita que las moléculas de jabón emulsionen la grasa a menos que se use un exceso grande.
Los detergentes como los alquilbencenosulfonatos (ABS) y los alquilbencenosulfonatos lineales (LAS) tienen estructuras muy similares al estearato de sodio, excepto que el grupo cargado en sus cabezas hidrofílicas está —SO3– unido a un anillo de benceno. Los detergentes ABS también tienen grupos metilo (CH3) que se ramifican de sus cadenas de hidrocarburos.,
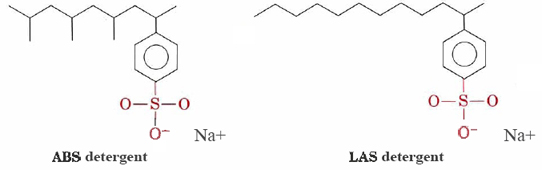
tales moléculas no precipitan con cationes de agua dura y, por lo tanto, son más adecuadas para el lavado a máquina de la ropa. Los detergentes LAS reemplazaron a los ABS a mediados de los años sesenta, cuando se descubrió que estos últimos no eran biodegradables. Estaban haciendo que los ríos e incluso el agua del grifo se cubrieran con espuma y detergente. Aparentemente, las enzimas de los microorganismos que habían evolucionado para descomponer las cadenas de hidrocarburos no ramificadas en las grasas naturales y los ácidos grasos eran incapaces de digerir las cadenas ramificadas de las moléculas de ABS., Los detergentes LAS, aunque fabricados por humanos, imitan las estructuras de moléculas naturales y son biodegradables.