Einleitung
Typ-2-Diabetes mellitus (T2DM) zeichnet sich durch eine Insulinresistenz aus, die im Verlauf der Erkrankung relativ stabil bleibt, und einen fortschreitenden Verlust der β-Zellfunktion bei unzureichender Insulinsekretion., Aufgrund dieser fortschreitenden Entwicklung benötigen die meisten Patienten mit T2DM schließlich Insulin, um eine glykämische Kontrolle zu erreichen und aufrechtzuerhalten, wobei ein schrittweiser Ansatz verwendet wird, der mit Basalinsulin in Kombination mit oralen Mitteln beginnt. Wenn die präprandiale und postprandiale Glykämie nicht ausreichend kontrolliert wird, wird als nächster Schritt ein zweimal tägliches Insulinregime mit NPH (neutralem Protamin Hagedorn) oder vorgemischten Insulinpräparaten bevorzugt., Wie bei Typ-1-Diabetikern sollte eine Basal-Bolus-Insulintherapie bei T2DM-Patienten mit schwerem Insulinmangel angezeigt sein, die keine glykämischen Ziele mit zweimal täglichem Regime erreichen und aufrechterhalten können.1 Dieses Insulinregime wird jedoch eindeutig zu wenig angewendet, wahrscheinlich aufgrund der Zurückhaltung von Patienten und Ärzten aufgrund der Komplexität seiner Einrichtung sowie der begrenzten verfügbaren Informationen über die Durchführbarkeit, insbesondere bei älteren Probanden, und seiner Wirksamkeit bei Patienten, die zuvor mit zwei Insulindosen behandelt wurden.,2
In der vorliegenden Studie haben wir die Machbarkeit, Wirksamkeit und Sicherheit der Basal-Bolus-Insulintherapie bei Patienten mit langfristigem Typ-2-Diabetes und schlechter oder instabiler glykämischer Kontrolle bewertet.
Material und Methoden
In dieser prospektiven Einzelzentrumsstudie nahmen wir 37 Patienten auf, die von Oktober 2006 bis Oktober 2007 auf Basal-Bolus-Insulin umgestellt wurden und in den letzten sechs Monaten trotz Intervention zur Verbesserung eine instabile oder schlechte glykämische Kontrolle (glykiertes Hämoglobin (HbA1c)≥8%) hatten., Das Studienprotokoll wurde von den Institutional Ethics Review Boards genehmigt und die schriftliche Zustimmung aller Patienten eingeholt.
In der Anfangsbehandlung wurden Kohlenhydrate auf die drei Hauptmahlzeiten verteilt. Die anfängliche Insulin-Glargin-Dosis wurde als 50% der vorherigen gesamten Tagesdosis und das anfängliche Prandialinsulin (Aspart oder Lispro) als die restlichen 50% der gesamten Tagesdosis berechnet, die gleichmäßig auf die drei Mahlzeiten aufgeteilt wurde., Patienten, die vor dem Wechsel der Therapie Metformin einnahmen und keine Kontraindikation hatten, setzten die Anwendung in derselben Dosis fort. Die anderen oralen Antidiabetika wurden abgesetzt.
Alle Patienten nahmen an einem strukturierten ambulanten Diabetes-Trainingsprogramm teil, das aus drei 2-h-Gruppensitzungen in einer Woche für 5-8 Patienten bestand. Im Allgemeinen wurde ihnen beigebracht, eine Diät einzuhalten, bei der bei jeder Mahlzeit eine qualitative Kohlenhydrataufnahme vorausgesetzt wurde, obwohl bei Patienten, die diese variieren wollten, die Kohlenhydratzählung durchgeführt werden musste., Die Patienten lernten auch das Management der Basal-Bolus-Therapie und die Anpassung der Basalinsulindosen an den Fasten-selbstüberwachenden Blutzucker (SMBG) alle 7 Tage. Die Anpassung der prandialen Insulindosis wurde gemäß den Werten vor der Mahlzeit unter Verwendung eines einfachen Algorithmus mit festgelegten Dosen von schnell wirkendem Insulin durchgeführt. Die Patienten folgten den Besuchen der Krankenschwester nach 1 und 3 Wochen, 3 und 6 Monaten und des Endokrinologen nach 2, 4 und 7 Monaten, wobei die Ernährung überprüft und das Tagebuch mit SMBG-Werten überprüft wurde, um die Insulindosen anzupassen., Anthropometrische Daten (Gewicht, Body-Mass-Index und Taillenumfang) sowie Behandlungs-und biochemische Variablen wurden zu Studienbeginn und nach 3 und 6 Monaten bei allen Patienten erhalten. Wir quantifizierten den Insulinbedarf und die Anzahl schwerer Hypoglykämie (definiert als hilfebedürftig) anhand einer Anamnese und einer Überprüfung der Patiententagebücher.
HbA1c wurde mittels Hochleistungsflüssigchromatographie (HPLC) (Bio-Rad Laboratories, München) mit einem Referenzbereich von 4,6-5,8% bestimmt., Cholesterin und Triglyceride wurden durch standardisierte enzymatische Methoden und High-Density-Lipoprotein-Cholesterin (HDLc) durch eine direkte Methode (Roche Diagnostics, Basel, Schweiz) bestimmt. Low-density-lipoprotein-Cholesterin (LDLc) war geschätzt durch die Friedewald-Formel (wenn Triglycerid-Werte waren
3.39 mmol/l) oder durch ultrazentrifugation. Apolipoprotein (Apo) B wurde durch eine inmunoturbidimetrische Methode (Tina-quant, Roche Diagnostics) und LDL-Größe durch Elektrophorese (2-16%) bestimmt., Die Lebensqualität wurde anhand eines krankheitsspezifischen Fragebogens gemessen, der in Spanien an die Diabetes-Lebensqualität (DCCT) zu Studienbeginn angepasst und 6 Monate nach der Basal-Bolus-Insulintherapie wiederholt wurde.3,4
Daten wurden vom statistischen Programm SPSS 15.0 (SPSS Inc.). Die änderungen in anthropometrical Variablen, HbA1c, insulin Anforderungen und lipid-Profil ausgewertet wurden durch die t-Student-test. Sie wurden als signifikante Werte von p≤0,05 angesehen.
Ergebnisse
Die klinischen Grundmerkmale sind in Tabelle 1 zusammengefasst., Achtundsiebzig Prozent der Patienten wurden mit 2 Dosen NPH oder vorgemischten Insulinpräparaten behandelt, 11% der Patienten nahmen orale Medikamente und Insulin vor dem Schlafengehen (Glargin, Detemir oder NPH) ein und die restlichen 11% der Patienten verwendeten andere Therapien mit 3 Dosen NPH und regelmäßigem Insulin. Siebenundachtzig Prozent der Patienten hatten eine HbA1c-Konzentration >8% und 51% hatten HbA1c>9%. Nach dem Wechsel zur Basal-Bolus-Therapie sank HbA1c nach 3 Monaten von 9±1,2% auf 8,1±1,2% (p
0,001) und nach 6 Monaten auf 8,0±1,2% (p0.001) (Tabelle 1, Abb. 1)., Der Prozentsatz der Patienten mit HbA1c≥9% sank von anfänglichen 51% (19 Probanden) nach 3 bzw. Abb. 2 zeigt den Anteil der Patienten mit einem HbA1c7%, 7-8% und >8% vor und nach dem Wechsel zur Basal-Bolus-Therapie. Fünf der Patienten zeigten eine Verschlechterung der HbA1c-Werte. Es wurde nur eine Episode einer schweren Hypoglykämie registriert. Nach 6 Monaten konnten alle Patienten die Basalinsulindosis anpassen, aber nur 10 Patienten modifizierten die Prandialdosis gemäß den Mustern von SMBG autonom.,
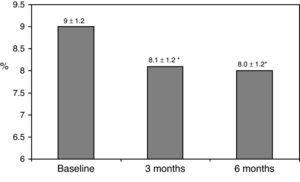
Glycated hemoglobin at baseline and 3 and 6 months after switching to basal-bolus regimen. *p0.001 compared to baseline. HbA1c: glycated hemoglobin.
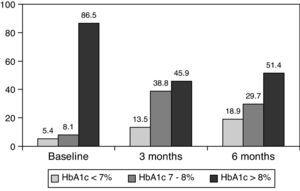
Percentage of patients with glycated hemoglobin 8% at baseline, and 3 and 6 months after switching to basal-bolus regimen.
Körpergewicht, Insulinbedarf und Lipidparameter zu Studienbeginn und während der Nachsorge sind in Tabelle 1 dargestellt. Das Körpergewicht blieb während der 6-monatigen Nachbeobachtung stabil und der Insulinbedarf (UI/kg/Tag) änderte sich nach 3 Monaten nicht und stieg nach 6 Monaten leicht an. Die Größe der LDL-Partikel deutlich erhöht auf 3 (25.77±0.48 nm vs 25.98±0.5 nm, p0.05) und 6 Monate (25.77±0.48 nm vs 25.94±0.44 nm, p0.05), während die andere lipidic Parameter nicht ändern.,
Diskussion
In der vorliegenden Studie haben wir gezeigt, dass die Basal-Bolus-Insulintherapie eine Verbesserung der Blutzuckerkontrolle ermöglicht, ohne die Sicherheit und Lebensqualität bei Patienten mit langfristigem Typ-2-Diabetes zu beeinträchtigen, die zuvor mit einer oder mehreren Insulindosen behandelt wurden. Wir zeigen auch die Machbarkeit der Umsetzung dieser Insulinregime durch ein strukturiertes ambulantes Trainingsprogramm.,
Konsensrichtlinien für die Behandlung von Typ-2-Diabetes sind der Ansicht, dass die primären Behandlungsziele darin bestehen, die HbA1c-Konzentrationen so niedrig wie möglich zu erreichen, ohne eine inakzeptable Hypoglykämie zu verursachen, insbesondere bei älteren Patienten oder bei koronaren Erkrankungen, und die Entwicklung von mikrovaskulären und makrovaskulären Komplikationen zu verhindern.1.5 Leider zeigen jüngste Umfragen, dass ein großer Teil der Patienten mit Diabetes die empfohlenen glykämischen Ziele nicht erreicht.,6,7 Obwohl in der National Health and Nutrition Examination Survey (NHANES) der Anteil der Patienten mit HbA1c
7% von 37% in den Jahren 1999-2000 auf 56,8% in den Jahren 2003-2004 gestiegen ist, sind die Raten der suboptimalen glykämischen Kontrolle besonders hoch bei Personen mit ähnlichen Eigenschaften wie bei uns, die über eine langjährige Diabetes-oder Insulinbehandlung verfügen.,6,7 Zweimal tägliche Dosen mit NPH oder vorgemischtem Insulin werden verwendet, um Insulinschemata zu vereinfachen, haben jedoch eine begrenzte Flexibilität, erfordern eine starre Einhaltung regelmäßiger Mahlzeiten, begrenzen die Fähigkeit, die Dosierungen der einzelnen Komponenten anzupassen und erhöhen die Möglichkeit einer Hypoglykämie. Obwohl viele Patienten zunächst mit diesem Regime eine ausreichende Blutzuckerkontrolle erreichen, 8 wenn die Insulinsekretionskapazität der Betazellen verloren geht und der Insulinmangel schwerwiegend ist, wird die Blutzuckerkontrolle wie bei den meisten Patienten, die in die vorliegende Studie einbezogen sind, schlecht und instabil.,1,8 Wir zeigten, dass bei Patienten mit langfristigem Typ-2-Diabetes, die mit anderen Insulinschemata und instabilem Profil schlecht kontrolliert wurden, das Basal-Bolus-Insulinregime HbA1c um einen Punkt über 6 Monate und den Anteil der Patienten mit HbA1c≥9% von 51% auf 14% nach 3 Monaten und 19% nach 6 Monaten reduziert. Dies liegt wahrscheinlich daran, dass es sich um eine physiologischere Therapie handelt; Während prandiales Insulin die endogene Insulinsekretion in der ersten Phase ersetzt, verringert Basalinsulin das Niveau der Fastenhyperglykämie., So verändert die Art und Weise, wie die Behandlung intensiviert wird, zusätzlich zum HbA1c-Spiegel die relativen Beiträge der basalen und postprandialen Hyperglykämie zur allgemeinen Hyperglykämie von T2DM-Patienten erheblich. Vor kurzem, Riddle et al.10 zeigte, dass nach Intensivierung der Behandlung mit Insulin der Beitrag der basalen Hyperglykämie abnimmt, aber immer noch etwa ein Drittel der verbleibenden Hyperglykämie ausmacht. Nach den Ergebnissen der vorliegenden Studie ist daher häufig die Verwendung von Insulinschemata erforderlich, die basales mit prandialem Insulin kombinieren, um glykämische Ziele zu erreichen., Tatsächlich stimmen diese Ergebnisse mit den umfangreichen Nachweisen für die Vorteile der Basal-Bolus-Therapie bei Typ-1-Diabetes 11 überein und werden durch die begrenzten Daten aus Beobachtungsstudien bei Patienten mit Typ-2-Diabetes, die von einer Vormischung zu einer Basal-Bolus-Glargin-basierten Therapie wechseln 12,13 und durch einen randomisierten Vergleich einer Vormischung mit einer Basal-Bolus-Therapie bei Typ-2-Diabetikern.2,14,15 Bei Patienten, die zuvor mit Glargin plus oralen Antidiabetika behandelt wurden, betrug der Unterschied bei HbA1c 0.,22% befürworten das Basal-Bolus-Glargin-basierte Regime im Vergleich zu einem vorgemischten Insulinregime15. In der PREFER-Studie 14 zeigte die Untergruppe der Patienten, die zuvor ein Basalinsulinregime erhielten, eine größere HbA1c-Reduktion mit Detemir/Aspart Basal-Bolus-Regime im Vergleich zu biphasischem Insulin Aspart (-1.21% vs -0.75%). Schließlich bei premix behandelten Typ-2-Diabetikern Fritsche et al. zeigte, dass ein Basal-Bolus-Glargin / Glulisin-basiertes Insulinregime einem Vormisch-Insulinregime bei der Reduktion von HbA1c überlegen war (-1.31% gegenüber 0.8%).,2 Daher scheint die Überlegenheit eines Basal-Bolus-Regimes bei ausgewählten Patienten mit langjähriger Erkrankung nachgewiesen zu sein, obwohl es Unterschiede im Ausmaß der Verbesserung zwischen den Studien gibt, wahrscheinlich aufgrund der unterschiedlichen Grundlinienmerkmale der untersuchten Population. Die Reduktion von mehr als einem Punkt von HbA1c, der durch die Umstellung auf ein Basal-Bolus-Insulin-Regime erreicht wird, kann als klinisch signifikant angesehen werden, da dies zu einer Verringerung der klinischen Ergebnisse führen kann., Leider wird die Basal-Bolus-Therapie bei Patienten mit T2DM zu wenig angewendet, da Ärzte sie für komplex halten, zeitaufwendig sind und Befürchtungen vor einer erhöhten Anzahl von Injektionen, einem Risiko für Hypoglykämie, Gewichtszunahme und einer Verschlechterung der Lebensqualität bestehen. In dieser und früheren Studien wurden das Körpergewicht und die Rate schwerer Hypoglykämie nicht erhöht,2,12 was mit der physiologischeren Insulinsubstitution mit Basal-Bolus-Regime und der Flexibilität zusammenhängen könnte, die diese Therapie den Patienten bieten kann., Daher sollte die Angst vor Hypoglykämie kein Hindernis sein, um diese Art von Therapie bei T2DM zu beginnen, aber sie muss berücksichtigt werden, um glykämische Kontrollziele festzulegen, da sie Morbidität und erhöhte Mortalität verursachen können.16 Bezüglich der Auswirkungen auf die Lebensqualität im Einklang mit dem Bericht von Ménard et al.,17 unsere Studie unterstützte nicht die Ansicht, dass Basal-Bolus-Therapien zu einer verminderten Lebensqualität führen.
Einem früheren Bericht zufolge konnten 12 in der vorliegenden Studie alle Patienten ihre Basalinsulindosis gemäß dem Fasten-SMBG der letzten 3-7 Tage titrieren., Im Gegensatz dazu waren nur wenige Patienten in der Lage, die prandialen Insulindosen gemäß den Mustern von SMBG anzupassen, und die meisten benötigten die Unterstützung eines einfachen Algorithmus mit einer festgelegten Dosis in Abhängigkeit vom prämealen Blutzucker. Dies ist nicht verwunderlich, da die Festlegung der optimalen Insulindosis zu den Mahlzeiten häufig Berechnungen beinhaltet, die mehrere Faktoren berücksichtigen und für einige Patienten schwierig sind. Darüber hinaus ist die Verwendung eines einfachen Algorithmus zur wöchentlichen Anpassung von schnell wirkendem Insulin für die Mahlzeiten anhand von SMBG-Mustern genauso effektiv wie die Anpassung von Insulin für die Mahlzeiten unter Verwendung von Insulin-Kohlenhydrat-Verhältnissen bei T2DM-Probanden.,18
Einschränkungen der Studie beziehen sich auf das prospektive Beobachtungsdesign und das Fehlen einer Kontrollgruppe. Diese Aspekte und die kurze Nachsorge von Patienten, die schwer zu interpretieren sind, die Befunde und ihre Anwendbarkeit auf Patienten mit T2DM folgten in anderen Zentren. Obwohl zukünftige Studien an größeren Patientengruppen durchgeführt werden sollten, um diese Ergebnisse zu bestätigen, liefert die Studie Informationen, die für das Management einer häufigen und schlecht behandelten klinischen Situation nützlich sein können.,
Abschließend zeigte die vorliegende Studie, dass ein 9-stündiges ambulantes Programm es T2DM-Patienten mit langer Dauer, die mit anderen Insulinschemata schlecht kontrolliert wurden, ermöglichte, auf ein Basal-Bolus-Insulinregime umzusteigen. Wir haben auch bestätigt, dass das Basal-Bolus-Insulin-Regime wirksam, sicher und die Lebensqualität in dieser Untergruppe von T2DM-Patienten nicht beeinträchtigt. Daher könnte eine Basal-Bolus-Therapie für T2DM-Probanden angeboten werden, die mit anderen Insulinstrategien unzureichend kontrolliert werden.
Interessenkonflikt
Irene Vinagre hat Vorlesungsgebühren von Eli Lilly, Novo Nordisk und Sanofi Aventis erhalten., Antonio Perez hat con sulting und Vorlesungsgebühren von Eli Lilly, Novo Nordisk und Sanofi Aventis erhalten.