cíle učení
- pravidlo státu Hund.
- aplikujte Hundovo pravidlo na plnění orbitálů.
- použijte orbitální plnicí diagramy k popisu umístění elektronů v atomu.
Přemýšleli jste někdy, co znamenají tyto značky omezení zatížení na mostě?
výše uvedený znak říká, že nic nad pět tun není povoleno, protože způsobí poškození konstrukce., Existují limity na množství hmotnosti, které může most podporovat, existují limity pro počet lidí, kteří mohou bezpečně obsadit místnost, a existují limity toho, co může jít do elektronového orbitalu.

Hund je Pravidlo
poslední tři pravidla pro výstavbu elektronového uspořádání vyžaduje elektrony, které mají být umístěny po jednom v sadu orbitalů ve stejném podlaží. To minimalizuje přirozené odpudivé síly, které má jeden elektron pro druhého., Hundovo pravidlo uvádí, že orbitaly stejné energie jsou každý obsazeny jedním elektronem, než je jakýkoli orbital obsazen druhým elektronem a že každý z jednotlivých elektronů musí mít stejnou rotaci. Níže uvedený obrázek ukazuje, jak je sada tří P orbitalů naplněna jedním, dvěma, třemi a čtyřmi elektrony.
orbitální Plnicí diagramy
orbitální plnicí diagram je vizuálnější způsob, jak reprezentovat uspořádání všech elektronů v určitém atomu., V orbital plnění schéma, jednotlivé orbitaly jsou zobrazeny jako kruhy (nebo čtverce) a orbitaly v mezipatře jsou nakresleny vedle sebe horizontálně. Každá podúroveň je označena svou hlavní energetickou úrovní a podúrovní. Elektrony jsou označeny šipkami uvnitř kruhů. Šipka směřující nahoru označuje jeden směr otáčení, zatímco šipka směřující dolů označuje druhý směr. Orbitální plnicí diagramy pro vodík, helium a lithium jsou uvedeny na obrázku níže.
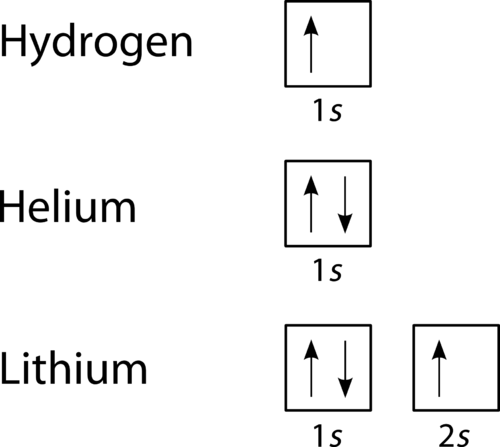
Obrázek 2., Orbitální plnicí diagramy pro vodík, helium a lithium.
podle procesu Aufbau jsou podúrovně a orbitaly naplněny elektrony v pořadí zvyšující se energie. Vzhledem k tomu, že s podúroveň se skládá pouze z jednoho orbitalu, druhý elektron se jednoduše spáruje s prvním elektronem jako v héliu. Dalším prvkem je lithium a vyžaduje použití další dostupné podúrovně, 2S.
plnicí diagram pro uhlík je znázorněn na obrázku níže. Existují dva 2 p elektrony pro uhlík a každý zaujímá svůj vlastní 2 P orbital.,
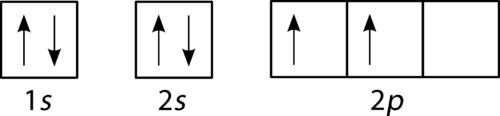
obrázek 3. Orbitální plnicí diagram pro uhlík.
kyslík má čtyři 2 p elektrony. Po každém 2 P orbital má jeden elektron v něm, čtvrtý elektron může být umístěn v prvním 2 P orbitalu s odstřeďováním naproti tomu druhého elektronu v tomto orbitalu.
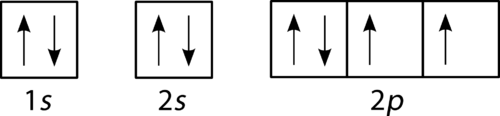
obrázek 4. Orbitální plnicí diagram pro kyslík.
Shrnutí
- Hund je pravidlo určuje pořadí elektron plnění ve stanovené orbitalů.,
- orbitální plnicí diagramy jsou způsob, jak indikovat umístění elektronů v orbitálech.
Cvičení
Použijte odkaz níže provádět následující cvičení:
https://www.caymanchem.com/app/template/chemAssistant,Nástroj.vm / itemid / 4001
- Vyberte atom ze seznamu (pravděpodobně budete chtít udělat nižší atomová čísla). Nechte číslo nastavit nulu.
- vyhledejte atom v periodické tabulce a určete počet přítomných elektronů.
- nakreslete schéma orbitální náplně atomu.,
- klikněte na tlačítko „Vypočítat“a porovnejte svou odpověď s odpovědí.
Review
- State Hundovo pravidlo.
- co je orbitální plnicí diagram?
- je diagram na obrázku níže správný? Vysvětlete svou odpověď.

- je diagram na obrázku níže správný? Vysvětlete svou odpověď.,

Slovníček pojmů
- Hund je pravidlo: Orbitaly o stejné energii jsou každé obsazené jedním elektronem, než jakékoli orbital je obsazený druhý elektron a že jednotlivé elektrony, musí mít stejný spin.
- orbitální plnicí diagram: vizuální způsob, jak reprezentovat uspořádání všech elektronů v určitém atomu.