β-Hydroxybutyrat ist einer der Ketonkörper. Siehe das Bild unten.
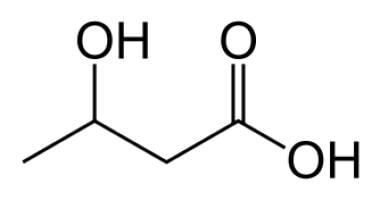 Beta-hydroxybutyrat.
Beta-hydroxybutyrat. Der Begriff Ketonkörper beschreibt 3 Moleküle: Acetoacetat, β-Hydroxybutyrat und Aceton. Acetoacetat wird durch Acetyl-CoA-Metabolismus produziert, β-Hydroxybutyrat ist das Ergebnis der Acetoacetatreduktion und Aceton wird durch spontane Decarboxylierung von Acetoacetat produziert., Ketonkörper sind grundlegend für die metabolische Homöostase während längerer Hungerszeiten. Das Gehirn kann keine Fettsäuren für die Energieproduktion verwenden und hängt normalerweise von Glukose ab, um seinen metabolischen Bedarf zu decken. In Fällen von Fasten oder Hunger werden Ketonkörper zu einem Hauptbrennstoff für Gehirnzellen und schonen Aminosäuren davor, zu Glukoneogenese-Vorläufern katabolisiert zu werden, um das Gehirn mit Energie zu versorgen. Nach längerem Verhungern können Ketonkörper bis zu zwei Drittel des Energiebedarfs des Gehirns decken.,
Ketonkörper sind starke organische Säuren, die sich im Blut vollständig dissoziieren. Wenn die Ketonkörperproduktion unkontrollierbar wird, sind die Puffersysteme gesättigt und der Blut-pH-Wert sinkt; Dies ist ein Zustand, der als Ketoazidose bekannt ist. Die beiden häufigsten klinischen Szenarien für Ketoazidose sind diabetische Ketoazidose und alkoholische Ketoazidose.
Diabetische Ketoazidose
Die klinisch relevanteste Anwendung der β-Hydroxybutyrat-Bestimmung umfasst die Diagnose, das Management und die Überwachung der diabetischen Ketoazidose., Bei Insulinmangelzuständen führt die Lipolyse im Fettgewebe (stimuliert durch Insulinmangel) zu einer enormen Fettsäurebelastung der Leber. Fettsäuren werden zunächst zu Acetyl-Coenzym A metabolisiert, das aufgrund eines Oxaloacetatmangels nicht in den Zitronensäurekreislauf in den Mitochondrien gelangen kann. So wird Acetyl-Coenzym A durch die Aktivität mehrerer Enzyme, die Acetoacetat produzieren, zur Ketonkörperproduktion umgeleitet. Acetoacetat wird dann durch 3-β-Hydroxybutyrat-Dehydrogenase zu 3-β-Hydroxybutyrat-Dehydrogenase reduziert.,
Das Verhältnis von Acetoacetat zu 3-β-Hydroxybutyrat hängt vom Redoxstatus in den Lebermitochondrien ab (dh vom NAD+/NADH-Verhältnis). Unter normalen Umständen liegt das Verhältnis von β-Hydroxybutyrat zu Acetoacetat bei etwa 1; Bei diabetischer Ketoazidose kann dies jedoch auf 7-10 ansteigen. Aceton wird durch spontane Decarboxylierung von Acetoacetat hergestellt.,
Traditionell basierte die Diagnose einer diabetischen Ketoazidose auf dem Nachweis von Ketonen im Urin unter Verwendung der legalen Reaktion, bei der Acetoacetat in Gegenwart von Alkali mit Nitroprussid reagiert, um einen violetten Komplex auf einem Teststreifen zu erzeugen. Diese Methode hat jedoch erhebliche Nachteile. Es ist semiquantitativ und nicht gleich empfindlich für Urin und Blut.
Darüber hinaus sind nicht alle Patienten mit diabetischer Ketoazidose in der Lage, eine Urinprobe bei der Präsentation bereitzustellen, und Ketone im Urin sind keine genaue Schätzung von Blutketonen., Am wichtigsten ist, dass der am häufigsten vorkommende Ketonkörper bei diabetischer Ketoazidose β-Hydroxybutyrat ist, dessen Konzentration 3-10 mal höher ist als die von Acetoacetat. Wenn eine diabetische Ketoazidose behandelt wird, wird Serum-β-Hydroxybutyrat aufgrund der Korrektur des mitochondrialen Redoxstatus in Acetoacetat umgewandelt, wodurch der Acetoacetatspiegel im Urin erhöht wird und der falsche Eindruck entsteht, dass der Patient nicht auf die Behandlung angesprochen hat.,
Schließlich können Urin-Ketonstreifen bei Patienten, die Arzneimittel mit Sulfhydrylgruppen erhalten, falsch positive Ergebnisse und falsch negative Ergebnisse liefern, wenn sie längere Zeit Luft ausgesetzt waren oder wenn der Urin sauer ist. Diese Nachteile erfordern die Entwicklung einer zuverlässigeren Methode zur Diagnose und Behandlung von diabetischer Ketoazidose.
In einer signifikanten Anzahl von Studien wurde die Fähigkeit von Point-of-Care-β-Hydroxybutyrat zum Nachweis von Patienten mit diabetischer Ketoazidose bewertet., In verschiedenen Studien liegt der Grenzwert für die Diagnose einer diabetischen Ketoazidose zwischen 1,5 und 3,5 mmol/l, und das für die β-Hydroxybutyratmessung notwendige Blutvolumen beträgt 5-10 µL.
Ein β-Hydroxybutyratspiegel von mehr als 1,5 mmol/l hatte eine Empfindlichkeit von 98-100% und eine Spezifität von 78,6-93,3% für die Diagnose einer diabetischen Ketoazidose bei Diabetikern, die sich mit Blutzuckerspiegeln von mehr als 250 mg/dl an der ED präsentierten., In 2 anderen großen Studien hatte ein Grenzwert von 3 mmol/L bei Patienten, die sich der ED mit Hyperglykämie stellten, eine Empfindlichkeit von fast 100% und eine Spezifität von 92,89-94% für die Diagnose einer diabetischen Ketoazidose. Obwohl die meisten Hersteller eine Schwelle von 1,5 mmol/l vorschlagen, haben die Autoren eine Erhöhung des Grenzwerts auf 2 mmol/l oder sogar 3,5 mmol/l vorgeschlagen, um die diagnostische Ausbeute des Tests zu maximieren.,
Zahlreiche Studien haben die Überlegenheit von Blut-β-Hydroxybutyrat gegenüber Urinketonen bei Patienten mit Diabetes und Hyperglykämie mit möglicher diabetischer Ketoazidose gezeigt. Der Point-of-Care-β-Hydroxybutyrat-Test ist viel schneller als der klassische Urin-Keton-Test, kann bei der Ankunft leicht erhalten werden und hängt nicht von der Urinproduktion des Patienten ab. Während die Empfindlichkeit von Urinketonen ähnlich der von β-Hydroxybutyrat ist, hat sich gezeigt, dass letzteres persistent spezifischer für beide ist 1.,5 mmol/l und 3 mmol/L Endpunkte und hat auch einen größeren positiven Vorhersagewert.
Was die Überwachung der Behandlung betrifft, korrelieren β-Hydroxybutyratkonzentrationen im Vergleich zu Acetoacetat stärker mit Anionenlücke, pCO2 und Anionenlücke bei Patienten mit diabetischer Ketoazidose. In einer pädiatrischen Studie hat die Verwendung eines β-Hydroxybutyrat-Endpunkts zur Auflösung der diabetischen Ketoazidose (< 1 mmol/L) zu einer früheren ICU-Entladung (17 h vs 28 h) im Vergleich zur Standardbehandlung mit Urinproben geführt., In einer ähnlichen, medizinisch-ökonomischen Untersuchung führte die Verwendung eines β-Hydroxybutyrat-Endpunkts bei Kindern mit diabetischer Ketoazidose zu einer Verkürzung der Verweildauer auf der Intensivstation um 6,5 Stunden, 375 weniger Laboruntersuchungen pro Patient und einer kumulativen Abnahme von 2.950 Euro pro Patient, ohne die Patientensicherheit zu beeinträchtigen.
In einer pädiatrischen Studie hat die routinemäßige Durchführung der Blut-β-Hydroxybutyrat-Überwachung für die Behandlung von Krankheitstagen und die Behinderung der Ketoazidose den Krankenhausaufenthalt im Vergleich zur üblichen Praxis der Urinketonmessung verringert.,
Alkoholische Ketoazidose
Dies ist die zweithäufigste Ursache für Ketoazidose, wenn auch deutlich seltener als diabetische Ketoazidose. In den meisten Fällen berichten Patienten von einem signifikanten Alkoholkonsum, der mit Fasten einhergeht. Aus biochemischer Sicht wird Ethanol zu Acetoacetat und dann zu Acetat metabolisiert, wodurch signifikante Mengen an NADH produziert werden. Um NAD+ zu regenerieren, wird Pyruvat zu Laktat metabolisiert und Oxaloacetat wird konsumiert, um Malat zu produzieren, wodurch Gluconeogenese-Vorläufer abgebaut werden., Während des Hungers sind die Insulinspiegel extrem niedrig und erleichtern den Eintritt von Acyl-CoA in Mitochondrien, wodurch erhebliche Mengen an Acetyl-CoA produziert werden, die im Krebs-Zyklus nicht metabolisiert werden können und in Richtung Ketonkörpersynthese umgeleitet werden.
Bei alkoholischer Ketoazidose ist das Verhältnis von β-Hydroxybutyrat zu Acetoacetat extrem hoch und β-Hydroxybutyratspiegel können bei der Diagnose und Behandlung von alkoholischer Ketoazidose nützlich sein., Es wurden jedoch keine Studien durchgeführt, um β-Hydroxybutyrat (Serum oder Blut) tatsächlich mit den traditionellen diagnostischen Parametern für alkoholische Ketoazidose zu vergleichen, und daher können keine Empfehlungen für oder gegen seine Verwendung in dieser Einstellung abgegeben werden.