Ein gutes Beispiel für ein unpolares Lipid ist das neutrale Fettglyceroltristearat. Diese häufigste Form von tierischem Fett dient als Energiespeicher und als Isolierung gegen Wärmeverlust. Auf molekularer Ebene besteht es aus drei Molekülen Stearinsäure und einem Glycerin:
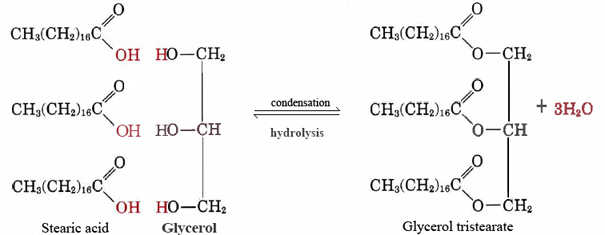 (1)
(1)
Durch die Kombination verschiedener langkettiger Säuren mit Glycerin können sehr viele unpolare Lipide hergestellt werden., Da diese Säuren ursprünglich aus Fetten gewonnen wurden, werden sie gemeinsam als Fettsäuren bezeichnet.
Beachten Sie, dass für jedes Stearinsäure —oder andere Fettsäuremolekül, das sich mit einer der OH-Gruppen von Glycerin verbindet, ein Molekül Wasser abgegeben wird und die Reaktion eine Kondensation ist. Es stellt sich heraus, dass sehr viele wichtige biologische Moleküle durch Kondensationsreaktionen zusammengesetzt werden, bei denen Wasser abgegeben wird. Die Rückseite von Eq. (1), in dem Wasser mit einem großen Molekül reagiert und es in kleinere Stücke aufspaltet, wird Hydrolyse genannt., Durch Hydrolyse können lebende Organismen Moleküle abbauen, die von anderen Spezies hergestellt werden. Die auf diese Weise erhaltenen einfachen Bausteine können dann durch Kondensationsreaktionen zu Strukturen rekombiniert werden, die ihrem neuen Wirt angemessen sind.
Im Gegensatz zu dem bei Tieren vorkommenden Glycerintristearat enthalten pflanzliche Fette zahlreiche Doppelbindungen in ihren langen Kohlenwasserstoffketten. Diese Polyunsättigung führt aufgrund der Drehbarriere und der mit den Doppelbindungen verbundenen 120° – Winkel „Knicke“ in die Kohlenwasserstoffketten ein., Folglich ist es schwieriger, die Ketten nebeneinander auszurichten (siehe Abbildung \(\pageIndex{1}\) ), und die ungesättigten Fette packen sich nicht so leicht in einem Kristallgitter zusammen. Wie bei Alkanen bestimmt auch die Kettenlänge, ob ein Fett flüssig oder fest ist und wo der Schmelzpunkt auftritt.
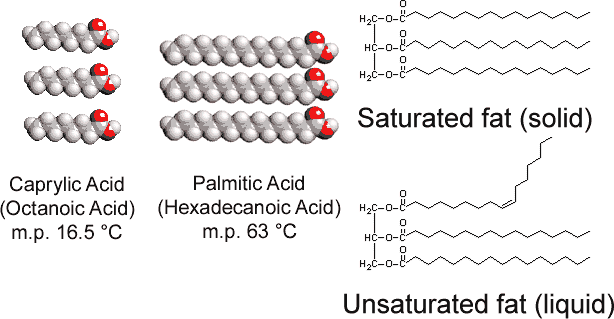
Die meisten ungesättigten Fette (wie Maisöl) sind Flüssigkeiten bei normalen Temperaturen, während gesättigte Fette (wie Butter) Feststoffe sind. Pflanzenöle können durch Hydrierung in Feststoffe umgewandelt werden. Bei diesem Prozess wird H2 katalytisch zu den Doppelbindungen hinzugefügt:
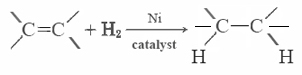
Bei der Herstellung von Seifen ist die Hydrolyse von Fetten wichtig., Es kann durch die Zugabe einer starken Base wie NaOH oder KOH beschleunigt werden, wobei die Reaktion als Verseifung bezeichnet wird. Da die Verseifung einen hohen pH-Wert des Reaktionsmischs erfordert, dissoziiert die produzierte Fettsäure zu ihrem Anion. Wenn Glycerintristearat beispielsweise mit NaOH verseift wird, bildet sich Natriumstearat, eine relativ wasserlösliche Substanz und eine übliche Seife.
Die Fähigkeit von Seifen, Fett und Öl von verschmutzten Oberflächen zu reinigen, ist ein Ergebnis der doppelten hydrophob-hydrophilen Strukturen ihrer Moleküle., Das Stearat-Ion besteht beispielsweise aus einer langen unpolaren Kohlenwasserstoffkette mit einer hochpolaren COO —Gruppe an einem Ende.
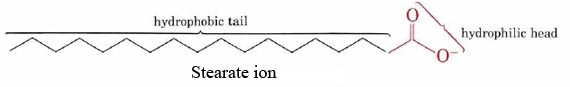
Die hydrophobe Kohlenwasserstoffkette versucht, den Kontakt mit wässrigen Medien zu vermeiden, während die anionische Gruppe die Dipolverbindungen und Wasserstoffbindungen von Wassermolekülen leicht aufnimmt.
Die beiden wichtigsten Möglichkeiten, wie die hydrophoben Anteile von Stearat-Ionen Wasser vermeiden können, bestehen darin, sich auf der Oberfläche anzusammeln oder sich in einer kleinen Menge Öl oder Fett aufzulösen (siehe Abbildung \(\pageIndex{2}\))).,
Im letzteren Fall berühren die hydrophilen Köpfe der Seifenmoleküle das Wasser außerhalb des Fettes und bilden eine Struktur, die als Mizelle bekannt ist. Da die Außenseiten der Mizellen negativ geladen sind, stoßen sie sich gegenseitig ab und verhindern ein Rekombinieren der Fetttröpfchen., Das Fett wird daher im Wasser suspendiert (emulgiert) und kann leicht abgewaschen werden.
Natürliche Seifen, wie Natriumstearat, wurden ursprünglich im Haushalt hergestellt, indem tierisches Fett mit Holzasche erhitzt wurde, die Kali, K2CO3 enthielt. Große Mengen werden noch industriell hergestellt, aber in erheblichem Maße wurden Seifen durch Reinigungsmittel ersetzt. Dies ist eine Folge des unerwünschten Verhaltens von Seifen in hartem Wasser. Calcium, Magnesium und andere Hartwasserkationen bilden in Kombination mit den Anionen von Fettsäuren unlösliche Verbindungen., Dies erzeugt düstere Niederschläge und verhindert, dass die Seifenmoleküle Fett emulgieren, es sei denn, es wird ein großer Überschuss verwendet.
Detergenzien wie Alkylbenzolsulfonate (ABS) und lineare Alkylbenzolsulfonate (LAS) haben Strukturen, die Natriumstearat sehr ähnlich sind, mit der Ausnahme, dass die geladene Gruppe in ihren hydrophilen Köpfen —SO3– an einem Benzolring befestigt ist. Die ABS-Detergenzien haben auch Methyl (CH3) – Gruppen, die sich von ihren Kohlenwasserstoffketten abzweigen.,
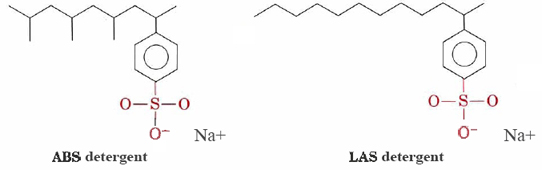
Solche Moleküle fallen nicht mit Hartwasserkationen aus und eignen sich daher besser zum maschinellen Waschen von Kleidung. Die LAS-Reinigungsmittel ersetzten Mitte der sechziger Jahre ABS, als festgestellt wurde, dass letztere nicht biologisch abbaubar waren. Sie führten dazu, dass Flüsse und sogar Leitungswasser mit Waschmittel und Schaum bedeckt wurden. Anscheinend waren die Enzyme in Mikroorganismen, die sich entwickelt hatten, um die unverzweigten Kohlenwasserstoffketten in natürlichen Fetten und Fettsäuren abzubauen, nicht in der Lage, die verzweigten Ketten von ABS-Molekülen zu verdauen., LAS Detergenzien, obwohl vom Menschen hergestellt, imitieren die Strukturen von natürlich vorkommenden Molekülen und sind biologisch abbaubar.